
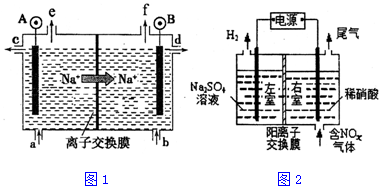
���� ��1���ɵ��ʳ��ˮװ��ͼ��֪�������������ұߣ������AΪ�������缫����ʽΪ2Cl--2e-=Cl2�����ұ�BΪ�������缫����ʽΪ2H2O+2e-=H2��+2OH- ��2H++2e-=H2�����������������ƴ�ͼ��dλ���������ݴ˷������
��2���ٸ���ͼ֪�����ʱ�������е缫�������ӷŵ�����������������Ϊ�����ң�����Ϊ�����ң�������ͨ����ǵ���������ɵ����ᣬ���������ϵ�������ʧ���Ӻ�ˮ�������
��n��NO2��=$\frac{2.24L}{22.4L/mol}$=0.1mol��������ӦʽΪNO2-e-+H2O=NO3-+2H+����0.2mol���������ɣ���Ϊ��0.1mol�������ɣ�����0.1mol���������������ң�
��3�����ݵ��ԭ�������������϶����������������������������������л������ӡ�Al2Cl7-��AlCl4-��ɵ�����Һ�������Һ��ʵ�֣�����AlCl3ˮ��Һ�����Һ����Һ���������������ŵ�����������
��� �⣺��1�����ɵ��ʳ��ˮװ��ͼ��֪�������������ұߣ������AΪ����������A��Ҫ���ӵ�Դ���������ʴ�Ϊ������
���ɵ��ʳ��ˮװ��ͼ��֪�������������ұߣ������AΪ�������缫����ʽΪ2Cl--2e-=Cl2�������Ծ��Ʊ���ʳ��ˮ��ͼ��aλ�ò��䣬�ұ�BΪ�������缫����ʽΪ2H2O+2e-=H2��+2OH- ��2H++2e-=H2�����������������ƴ�ͼ��dλ��������
�ʴ�Ϊ��a��d��
�۵���ܷ�Ӧ�����ӷ���ʽ��2Cl-+2H2O $\frac{\underline{\;ͨ��\;}}{\;}$ Cl2��+H2��+2OH-��
�ʴ�Ϊ��2Cl-+2H2O $\frac{\underline{\;ͨ��\;}}{\;}$ Cl2��+H2��+2OH-��
��2���ٸ���ͼ֪�����ʱ�������е缫�������ӷŵ�����������������Ϊ�����ң�����Ϊ�����ң�������ͨ����ǵ���������ɵ����ᣬ���������ϵ�������ʧ���Ӻ�ˮ�������ᣬ�缫��ӦʽΪ��NO2-e-+H2O=NO3-+2H+��
�ʴ�Ϊ��NO2-e-+H2O=NO3-+2H+��
��n��NO2��=$\frac{2.24L}{22.4L/mol}$=0.1mol��������ӦʽΪNO2-e-+H2O=NO3-+2H+����0.2mol���������ɣ���Ϊ��0.1mol�������ɣ�����0.1mol���������������ң�
�ʴ�Ϊ��0.1��
��3�������ݵ��ԭ�������������϶��������������������Դ�����������������������Դ�����������ʴ�Ϊ������
�����л������ӡ�Al2Cl7-��AlCl4-��ɵ�����Һ�������Һ��ʵ�֣�����Һ����һ�����������Σ�Ϊ��ˮ��ϵ����ƹ����в����������������л������Ӳ�����缫��Ӧ����������Ӧ�������Ƿ����Ļ�ԭ��Ӧ����Ԫ�ػ��ϼ۽��ͣ���������Һ��ɷ֣���ϵ���غ������֪��Al2Cl7-�õ��������ɣ��缫��ӦΪ��4Al2Cl7-+3e-=Al+7AlCl4-���ʴ�Ϊ��4Al2Cl7-+3e-=Al+7AlCl4-��
�۸���AlCl3ˮ��Һ�����Һ����Һ���������������ŵ�����������������ӦʽΪ2H++2e-=H2�����ʴ�Ϊ��2H++2e-=H2����
���� ���⿼����ԭ����Ϊ��Ƶ���㣬���ؿ���ѧ������������������ȷ�����缫�Ϸ����ķ�Ӧ�ǽⱾ��ؼ���ע�⣨2�����е�������ỹ����ԭ�������ᣬΪ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �ۢܢ� | C�� | �ۢݢ� | D�� | �ޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��������CO��ת��������������CO2��ת����֮��С��1 | |
| B�� | �������з�Ӧ��ƽ�ⳣ����ͬ | |
| C�� | ��������CO�����ʵ������������еĶ� | |
| D�� | ������������Ӧ������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ö��Ե缫��������Ȼ��ƣ�2Cl-+2H2O $\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2OH- | |
| B�� | ��������ϡ���2Fe+6H+�T2Fe3++3H2�� | |
| C�� | �� CuSO4��Һ���� H2S��Cu2++H2S�TCuS��+2H+ | |
| D�� | �� NH4HSO4 ��Һ�еμ������� Ba��OH��2��Һ��Ba2++2OH-+NH+H2O+H++SO2-�TBaSO4��+NH3•H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
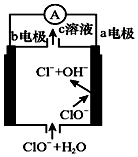
| A�� | ��ع���ʱ��c��Һ�е�����һ����MgCl2 | |
| B�� | ������Ӧʽ��ClO--2e-+H2O=Cl-+2OH- | |
| C�� | ��ع���ʱ��OH-��b�缫�ƶ� | |
| D�� | b�缫������ԭ��Ӧ��ÿת��0.1 mol���ӣ�����������0.1 mol Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� KIO3����������Һ�е� KI��5I-+IO3-+3H2O�T3I26OH- | |
| B�� | ��NH4��2Fe��SO4��2ϡ��Һ�м�һ����NaOH ��Һ��NH++2Fe2++5OH-�TNH3•H2O+2Fe��OH��2�� | |
| C�� | ���Ȼ�����Һ�е��������ˮ��Al3++3OH-�TAl��OH��3�� | |
| D�� | ������SO2ͨ��NaClO��Һ��SO2+H2O+2ClO-�TSO32-+2HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڶƼ��ϵ��ͭʱ�����ý���ͭ������ | |
| B�� | �Ʋ������������п���������������������ױ���ʴ | |
| C�� | ��ҵ�ϵ�ⱥ��ʳ��ˮ���ռNaOH���������� | |
| D�� | �����ڷ������ⸯʴ��������ʴʱ����ȫ��ͬ�ķ�Ӧ�Ǹ�����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com