
| A. | 已知25℃时NH4CN水溶液显碱性,则25℃时的电离平衡常数K(NH3•H2O)>K(HCN) | |
| B. | 25℃时,Mg(OH)2固体在20mL 0.01mol•L-1氨水中的KSP比在20mL 0.01mol•L-1NH4Cl溶液中的KSP小 | |
| C. | pH试纸测得新制氯水的pH为4.5 | |
| D. | NaHCO3溶液加热蒸干灼烧,得NaHCO3固体 |
分析 A.25℃时NH4CN溶液显碱性,则CN-的水解程度大于铵根离子的水解程度;
B.KSP只与温度有关;
C.新制氯水具有漂白性,不能用pH测定;
D.NaHCO3受热易分解.
解答 解:A.25℃时NH4CN溶液显碱性,说明CN-的水解程度大于铵根离子的水解程度,则25℃时的电离平衡常数K(NH3•H2O)>K(HCN),故A正确;
B.KSP只与温度有关,与浓度无关,所以25℃时,Mg(OH)2固体在20mL 0.01mol•L-1氨水中的KSP与在20mL 0.01mol•L-1NH4Cl溶液中的KSP相同,故B错误;
C.新制氯水具有漂白性,滴在pH试纸上,试纸会褪色,不能根据试纸的颜色变化来判断pH,不能用pH测定,故C错误;
D.NaHCO3溶液加热蒸干灼烧,由于NaHCO3受热易分解,最后得Na2CO3固体,故D错误.
故选A.
点评 本题考查较综合,涉及电离常数、溶度积常数、pH试纸的使用、碳酸氢钠的热稳定性等,把握发生的反应、电离与水解的判断为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:实验题
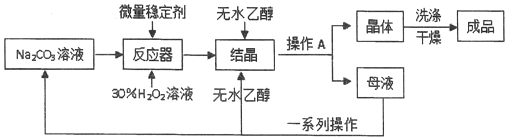
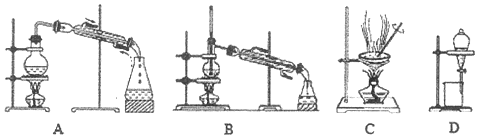

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发溶剂 | B. | 升高温度 | C. | 降低温度 | D. | 加入KN03固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I->Fe2+>Cl->SO2 | B. | Cl2>Fe3+>I2>SO2 | C. | Fe2+>I->Cl->SO2 | D. | Cl2>Fe3+>SO2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(CH3COOH):①>② | B. | c(CH3COO-):①>② | ||
| C. | c(CH3COOH)+c(CH3COO-):①=② | D. | c(CH3COO-)+c(OH-):①<② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1mol H2O的体积约为22.4L | |
| B. | 106g Na2CO3含有的Na+离子数为2 NA | |
| C. | 常温常压下,1 NA 个CO2分子占有的体积为22.4L | |
| D. | 1mol任何粒子的粒子数叫做阿伏加德罗常数,通常用6.02×1023表示 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com