
【题目】如图是关于反应A2(g)+3B2(g)2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( ) 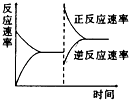
A.升高温度,同时加压
B.降低温度,同时减压
C.增大反应物浓度,同时减小生成物浓度
D.增大反应物浓度,同时使用催化剂
【答案】C
【解析】解:A、升高温度,同时加压,正逆反应速率都增大,逆反应速率应在原速率的上方,故A错误;
B、降低温度,同时减压正逆反应速率都降低,正反应速率应在原速率的下方,故B错误;
C、增大反应物浓度,同时减小生成物浓度,瞬间正反应速率增大,逆反应速率减小,平衡向正反应移动,图象符合,故C正确;
D、增大反应物浓度,同时使用催化剂,正逆反应速率都增大,逆反应速率应在原速率的上方,但正反应速率增大更多,平衡向正反应移动,故D错误.
故选:C.
【考点精析】本题主要考查了化学平衡状态本质及特征的相关知识点,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】在标准状况下①6.72L CH4②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3 , 下列对这四种气体的关系从大到小表达正确的是( )
A.体积②>③>①>④
B.密度②>③>①>④
C.质量②>①>③>④
D.氢原子个数①>③>②>④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.10g 46%的乙醇溶液所含氢原子数为1.2NA
B.0.5 mol熔融的NaHSO4中含有的离子数目为1.5NA
C.标准状况下,2.24L甲醇中含有C﹣H键的数目为0.3NA
D.S2和S8的混合物共38.4g,其中所含硫原子数为1.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与科技、社会、生产密切相关,下列事实不涉及化学反应的是
A.开采可燃冰生产天然气
B.利用二氧化碳生产燃料乙醇
C.化学家合成一些药物
D.利用石油生产塑料、化纤等高分子材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《菽园杂记》对海水提取食盐有如下记载:“烧草为灰,布在滩场,然后以海水渍之,侯晒结浮白,扫而复淋”。上述涉及的“灰”作用是( )
A.催化剂B.吸附剂C.氧化剂D.还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液含以下离子Na+、Mg2+、Ba2+、SO42-、I-、CO32-中的一种或几种,除水电离产生的H+、OH-外不含其他离子。为确定其组成进行以下实验,分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是( )
A.Na+B.SO42-
C.Ba2+D.Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298K时下述反应的有关数据:C(s)+ ![]() O2(g)=CO(g)△H1=﹣110.5kJmol﹣1 C(s)+O2 (g)=CO2(g),△H 2=﹣393.5kJ/mol 则C(s)+CO2(g)=2CO(g) 的△H为( )
O2(g)=CO(g)△H1=﹣110.5kJmol﹣1 C(s)+O2 (g)=CO2(g),△H 2=﹣393.5kJ/mol 则C(s)+CO2(g)=2CO(g) 的△H为( )
A.283.kJmol﹣1
B.172.5 kJmol﹣1
C.﹣172.5 kJmol﹣1
D.﹣504 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,aA(气)bB(气)达平衡后,保持温度不变,将容器体积增加1倍,当达到新平衡时,B的浓度是原来的60%,下列说法正确的是( )
A.平衡向逆反应方向移动了
B.物质A的转化率减少了
C.物质B的质量分数增加了
D.a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程: 
(1)固体I中主要成分为 , 捕获剂所捕获的气体主要是 .
(2)处理含NH4+废水时,发生反应的离子方程式为 .
(3)若X为适量空气,严格控制空气用量的原因是 .
(4)工业废气中的SO2、NO还可采用NaClO2溶液作为吸收剂进行净化,在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10﹣3molL﹣1 . 反应一段时间后溶液中离子浓度的分析结果如表:
离子 | SO42﹣ | SO32﹣ | NO3﹣ | NO2﹣ | Cl﹣ |
c(molL﹣1) | 8.35×10﹣4 | 6.87×10﹣6 | 1.5×10﹣4 | 1.2×10﹣5 | 3.4×10﹣3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式 .
增加压强,NO的转化率(填“提高”、“不变”或“降低”).
②随着吸收反应的进行,吸收剂溶液的pH逐渐(填“增大”、“不变”或“减小”).
③如果采用NaClO、Ca(ClO)2替代NaClO2 , 也能得到较好的烟气脱硫效果.从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com