
【题目】钠与水反应实验现象明显,下列不能观察到的实验现象是
A. 钠浮在水面上 B. 钠在水面上游动 C. 钠沉在水面下 D. 钠熔化成光亮小球
 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 37Cl和35Cl 互为同位素
B. 白磷和红磷互为同素异形体
C. C2H4和C3H6互为同系物
D. C2H5OH和CH3OCH3互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)在①苯 ②乙醇③甲苯 ④氯乙烷 ⑤![]() ⑥
⑥ ⑦
⑦![]() 七种物质中(填编号)
七种物质中(填编号)
能和金属钠反应放出H2的有_________________常温能与NaOH溶液反应的有___________
常温下能与溴水反应的有____________________能使酸性KMnO4溶液褪色的有__________
(2)某有机物结构简式如图所示,则用足量的Na、NaOH、NaHCO3、浓溴水分别与等物质的量的该有机物反应时,消耗Na、NaOH、NaHCO3和Br2的物质的量之比为__________.
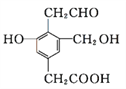
(3)A、B、C 三种醇同足量的金属钠完全反应,在相同条件下产生相同体积的氢气,消耗这三种醇的物质的量之比为2:6:3,则A、B、C 三种醇分子中含羟基数目之比是______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于钠的叙述中,不正确的是
A. 钠燃烧时发出黄色的火焰 B. 钠燃烧时生成氧化钠
C. 钠有很强的还原性 D. 钠原子的最外层只有一个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硫酸盐在工业生产中冇广泛的应用,某同学在实验中对亚硫酸盐的制备和性质进行探究。
(1)Cu2SO3·CuSO32H2O是一种深红色固体,不溶于水和乙醇,100℃时发生分解,其制备实验装置如图所示。

①仪器X的名称是________。常温下用装置A制取SO2时,用较浓的硫酸而不用稀硫酸,其原因是____________________。
②装置C的作用是________________________。
③装置B中发生反应的离子方程式为_____________________。
④从装置B中获得的固体需先用蒸馏水充分洗涤,再真空干燥,而不直接用烘干的方式得到产品,其原因是_________________________。
(2)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.NaHSO3和NaClO恰好反应;II.NaHSO3过量;III.NaClO过量。甲同学欲通过下列实验确定该反应属于哪一种情况,请完成下表:
实验操作 | 预期现象及结论 |
取上述反应后的混合溶液于试管 A中,滴加稀硫酸 | 若有气泡产生,则_①__(填“I”“II”或“III”,下同)成立,若没有气泡产生,则_②___成立 |
另取上述反应后的混合溶液于试管B中,滴加几滴淀粉KI溶液, 充分振荡 | ③___,则III成立 |
(3)请设计简单实验方案比较室温下NaHSO3浓液中HSO3-的电离平衡常数Ka与水解平衡常数Kb的相对大小:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g) ![]() 2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率 最快的是 ( )。
2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率 最快的是 ( )。
A. v(D)=0.4 mol·(L·s)-1 B. v(A)=0.15 mol·(L·s)-1
C. v(B)=0.6 mol·(L·s)-1 D. v(C)=0.5 mol·(L·s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如下图,依图所示:
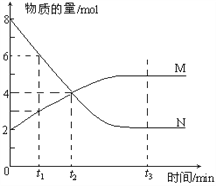
(1)该反应的化学方程式是_____________________。
(2)在图上所示的三个时刻中,_____(填t1、t2或t3)时刻处于平衡状态,此时V正____V逆(填>、<或=,);达到平衡状态后,平均反应速率v(N)﹕v(M)= _____。
(3)若反应容器的容积不变,则“压强不再改变”_______(填“能”或“不能”)作为该反应已达到平衡状态的判断依据。
(4)已知M、N均为气体,则下列措施能增大反应速率的是_____(选填字母)。
A.升高温度 B.降低压强 C.减小M的浓度 D.将反应容器体积缩小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计计如下图所示装罝(部分夹持装置己略去)进行实验探究:
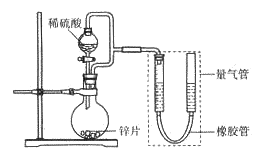
(1)用上述装置探究影响化学反应速率的因素。以生成9.0 mL气体为计时终点,结果为t1>t2。
序号 | V(H2SO4)/mL | C(H2SO4)/mol·L-1 | t/s |
I | 40 | 1 | t1 |
II | 40 | 4 | t2 |
①比较实验I和Ⅱ可以得出的实验结论是_______________。
②若将锌片换成含杂质的粗锌片,其他条件使其与上述一致,所测得的反应速率均大于上述实验对应的数据。粗锌片中所含杂质可能是_________(填序号)。
A.二氧化硅 B.银 C.铜 D.石墨
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀。
①圆底烧瓶中的试剂可选用________(填序号)。
A.稀HCl B .NaCl溶液 C.乙醇 D.NaOH溶液
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com