
【题目】下列关于晶体和非晶体的本质区别的叙述中,正确的是( )
A. 是否是具有规则几何外形的固体
B. 物理性质是否有各向异性
C. 是否是具有美观对称的外形
D. 内部构成微粒是否在空间呈有规则的重复排列
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知某元素原子的价电子排布式为(n-1)dansb,则下列说法正确的( )
A. 该元素是金属元素 B. 该元素位于周期表中d区
C. 该元素的族序数为a+b D. 该元素位于周期表中第四周期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类是学习和研究化学的一种重要方法,下列分类合理的是
A. H2SO4和HNO3都属于酸 B. K2CO3和K2O都属于盐
C. KOH和Na2CO3都属于碱 D. Na2O和Na2SiO3都属于氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢是一种理想的绿色清洁能源,氢气的制取与储存是氢能源利用领域的研究重点。 已知利用FeO与Fe3O4循环制氢的相关反应如下:
反应I. H2O(g)+3FeO(s) ![]() Fe3O4 (s) + H2(g) △H=a kJ mo1-1;
Fe3O4 (s) + H2(g) △H=a kJ mo1-1;
反应II 2 Fe3O4(s) ![]() FeO (s) + O2(g) △H=b kJ mo1-1。
FeO (s) + O2(g) △H=b kJ mo1-1。
(1) 反应:2H2O(g)=2H2(g)+O2(g) △H =________(用含 a、b的代数式表示)kJ mo1-1。
(2)上述反应中a<0、b>0,从能源利用及成本的角度考虑,实现反应II可采用的方案是________。
(3)900℃时,在甲、乙两个体积均为2.0 L的密闭容器中分别投入0.60 mol FeO(s)并通入0.20 mol H2O(g),甲容器用 FeO细颗粒,乙容器用FeO粗颗粒。反应过程中H2的生成速率的变化如图1所示。
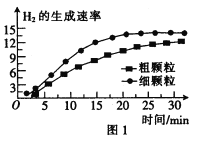
①用FeO细颗粒和FeO粗颗粒时,H2的生成速率不同的原因是__________。.
②用FeO细颗粒时H2O(g)的平衡转化率与用FeO粗颗粒时H2O(g)的平衡转化率的关系是___________(填“前者大”“前者小”或“相等”)。
(4)FeO的平衡转化率与温度的关系如图2所示。请在图3中画出1000℃、用FeO细颗粒时,H2O(g)转化率随时间的变化曲线(进行相应的标注)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究乙烯与溴的加成反应,甲同学设计并进行如下实验:先取一定量的工业用乙烯气体(在储气瓶中),使气体通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应;乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在工业上制得的乙烯中还可能含有少量还原性气体杂质,由此他提出必须先除去杂质,然后乙烯再与溴水反应。
请你回答下列问题。
(1)甲同学的实验中与乙烯有关的化学方程式为:______________________。
(2)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴发生加成反应,其理由是________。(填写序号)
①使溴水褪色的反应未必是加成反应
②使溴水褪色的反应就是加成反应
③使溴水褪色的物质未必是乙烯
④使溴水褪色的物质就是乙烯
(3)乙同学推测此乙烯中必定含有一种杂质气体是________,它与溴水反应的化学方程式是_______________。在验证过程中必须全部除去。除去该杂质的试剂可用________。
(4)为验证这一反应是加成反应而不是取代反应,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.增加反应物浓度可以增加单位体积活化分子数目,但活化分子百分数保持不变
B.升高温度可以提高活化分子的百分数,从而提高反应速率
C.对于任何反应,压缩容器容积来增大压强,反应速率都加快
D.催化剂可以降低反应所需要的活化能,提高活化分子的百分数,从而提高反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有溶质的物质的量浓度均为0.1 mol/L的下列八种溶液①HCl ②H2SO4 ③CH3COOH ④Ba(OH)2 ⑤KOH ⑥NaF ⑦KCl ⑧NH4Cl 这些溶液的pH由小到大的顺序是
A.②①③⑧⑦⑥⑤④ B.②①③⑥⑦⑧⑤④
C.①②③⑧⑦⑥④⑤ D.②①⑧③⑦⑥④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两瑞隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是( )
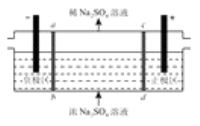
A.通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极反应为2 H2O–4e–=O2+4H+,负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com