

| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
A、氨气:N2+3H2
| ||||
B、铝:2Al2O3(熔融)
| ||||
C、氯气:MnO2+4HCl(浓)
| ||||
D、硫酸:2SO2+O2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为了提高甲烷与氯气的反应速率,用阳光直射反应容器 |
| B、为了验证甲烷与氯气的反应产物之一为氯化氢,水槽中改用AgNO3溶液 |
| C、用溴水鉴别乙烷和乙烯 |
| D、用高锰酸钾溶液除去乙烷中的乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
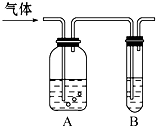 如图把气体缓慢通过盛有足量试剂的试剂瓶A,在试管B中可以观察到明显现象的是( )
如图把气体缓慢通过盛有足量试剂的试剂瓶A,在试管B中可以观察到明显现象的是( ) | 选项 | 气体 | A中试剂 | B中试剂 |
| A | SO2、CO2 | 酸性KMnO4溶液 | 品红溶液 |
| B | Cl2、HCl | 浓硫酸 | KI淀粉溶液 |
| C | NH3、CO2 | 浓硫酸 | 酚酞试液 |
| D | CO2、HCl | 饱和NaHCO3溶液 | AgNO3溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配制一定物质的量浓度的溶液时应先用该液体润洗容量瓶 |
| B、振荡分液漏斗时应关闭其玻璃塞和活塞 |
| C、蒸发结晶时蒸发皿应放在泥三角上 |
| D、锥形瓶用作反应容器时一定不能加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解后溶液的pH为1.7 |
| B、电解后溶液的pH为0.7 |
| C、该金属的相对原子质量是65 |
| D、以上结论均不正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com