
| A. | 将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,实现乙醇被氧化为乙醛的实验 | |
| B. | 相对分子质量相同的不同物质一定是同分异构体 | |
| C. | 淀粉和纤维素的分子式相同,所以两者互为同分异构体 | |
| D. | 可以用水鉴别硝基苯、乙醇、四氯化碳三种有机物 |
分析 A.加热变黑生成CuO,再与乙醇发生氧化反应;
B.相对分子质量相同的不同物质分子式不一定相同;
C.淀粉和纤维素的分子式不同;
D.硝基苯和四氯化碳的密度都比水大,且都不溶于水.
解答 解:A.加热变黑生成CuO,再与乙醇发生氧化反应,重复几次,完成乙醇氧化为乙醛的实验,实验合理,故A正确;
B.相对分子质量相同的物质,其分子式不一定相同,如乙醇与甲酸的相对分子量相同,但是二者的分子式不同,所以相对分子质量相同的不同物质不一定互为同分异构体,故B错误;
C.淀粉和纤维素都为高聚物,聚合度介于较大范围之间,没有固定的值,则二者的分子式不同,不是同分异构体,故C错误;
D.硝基苯和四氯化碳的密度都比水大,且都不溶于水,加入不能鉴别二者,故D错误.
故选A.
点评 本题综合考查有机物的结构和性质,为高考常见题型,题目涉及同分异构体的判断、有机物组成、结构与性质,难度不大,注意掌握常见有机物的结构与性质,明确相对分子量相同的有机物不一定具有相同的分子式.


科目:高中化学 来源: 题型:解答题
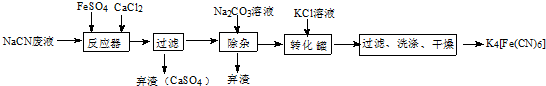
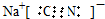 ;实验室用NaCN固体配制NaCN溶液时,应先将其溶于NaOH溶液,再用蒸馏水稀释.
;实验室用NaCN固体配制NaCN溶液时,应先将其溶于NaOH溶液,再用蒸馏水稀释.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作和现象 | 结论 |
| A | 向溶液中加入KSCN溶液无明显现象,再加入新制氯水,溶液呈血红色 | 证明原溶液中含有Fe2+ |
| B | 加入AgNO3溶液后生成白色沉淀,加稀盐酸沉淀不溶解 | 可确定有Cl-存在 |
| C | 将某种气体通入酸性KMnO4溶液.溶液褪色 | 说明该气体一定具有漂白性 |
| D | 向某溶液中逐渐通入CO2气体,先出现白色胶状沉淀,继续通入CO2气体,白色胶状沉淀不溶解 | 证明该溶液中存在AlO2- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑥ | B. | ①②③⑤ | C. | ①②④⑤ | D. | ①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 考古时可用12C测定一些文物的年代 | |
| B. | 可在元素周期表的过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料 | |
| C. | 乙烯是一种重要的基本化工原料,它的产量可以用来衡量一个国家的石油化工发展水平 | |
| D. | 红葡萄酒的密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | d为石墨,铁片腐蚀加快 | |
| B. | d为石墨,石墨上电极反应为:Na++e-═Na | |
| C. | d为锌块,铁片不易被腐蚀 | |
| D. | d为锌块,铁片上电极反应为:2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性氧化物都可以与强碱溶液反应 | |
| B. | 与水反应生成酸的氧化物都是酸性氧化物 | |
| C. | 金属氧化物都是碱性氧化物或两性氧化物 | |
| D. | 不能与酸反应的氧化物一定能与碱反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Mg2+ | B. | Mg2+、Fe2+ | C. | NH4+、Fe2+ | D. | Mg2+、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com