
【题目】化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成: 
已知:RCHO+CH3COOR′ ![]() RCH=CHCOOR′请回答:
RCH=CHCOOR′请回答:
(1)A中官能团的名称是;C→D的反应类型为;
(2)B+D→F的化学方程式;
(3)E的结构简式;
(4)对于化合物X,下列说法正确的是;
A.能发生水解反应
B.能发生银镜反应
C.不与浓硝酸发生取代反应
D.能使Br2的CCl4溶液褪色
(5)F有多种同分异构体,含有酯基和一取代苯结构的同分异构体有五个,其中四个的结构简式是: ![]() CH2CH2OOCH、
CH2CH2OOCH、 ![]() COOCH2CH3、
COOCH2CH3、 ![]() CH2COOCH3、
CH2COOCH3、 ![]() 00CCH2CH3 . 请写出另外一个同分异构体的结构简式 .
00CCH2CH3 . 请写出另外一个同分异构体的结构简式 .
【答案】
(1)羟基;取代反应
(2)![]()
(3)![]()
(4)AD
(5)![]() CH(CH3)OOCH
CH(CH3)OOCH
【解析】解:乙烯与水在催化剂作用下发生加成反应生成乙醇,故A是乙醇,乙醇催化氧化最终生成乙酸,故B是乙酸;甲苯在光照条件下与氯气发生的是取代反应,则C为 ![]() ,C在氢氧化钠的水溶液中发生的是取代反应,那么D应为
,C在氢氧化钠的水溶液中发生的是取代反应,那么D应为 ![]() ,由D能被氧化为E,且结合给出的信息:RCHO+CH3COOR′
,由D能被氧化为E,且结合给出的信息:RCHO+CH3COOR′ ![]() RCH=CHCOOR′,那么应E为
RCH=CHCOOR′,那么应E为 ![]() ,据此推断得出F为:
,据此推断得出F为: ![]() ,那么X为
,那么X为 ![]() ,(1)A是乙醇,A中官能团的名称是羟基;C→D的反应类型为取代反应, 所以答案是:羟基;取代反应;(2)B为乙酸,D为苯甲醇,两者发生酯化反应生成乙酸苯甲酯,化学反应方程式为:
,(1)A是乙醇,A中官能团的名称是羟基;C→D的反应类型为取代反应, 所以答案是:羟基;取代反应;(2)B为乙酸,D为苯甲醇,两者发生酯化反应生成乙酸苯甲酯,化学反应方程式为: ![]() ,
,
所以答案是: ![]() ;(3)根据上面的分析可知,E为
;(3)根据上面的分析可知,E为 ![]() ,
,
所以答案是: ![]() ;(4)A.X中含有酯基,能发生水解反应,故A正确;
;(4)A.X中含有酯基,能发生水解反应,故A正确;
B.X中不含有醛基,不能发生银镜反应,故B错误;
C.X中含有苯环,能与浓硝酸发生取代反应,故C错误;
D.X中含有碳碳双键,能使Br2/CCl4溶液褪色,故D正确,
故选AD;(5)F有多种同分异构体,含有酯基和一取代苯结构的同分异构体有五个,其中四个的结构简式是: ![]() CH2CH2OOCH、
CH2CH2OOCH、 ![]() COOCH2CH3、
COOCH2CH3、 ![]() CH2COOCH3、
CH2COOCH3、 ![]() 00CCH2CH3、
00CCH2CH3、 ![]() CH(CH3)OOCH,
CH(CH3)OOCH,
所以答案是: ![]() CH(CH3)OOCH.
CH(CH3)OOCH.


科目:高中化学 来源: 题型:
【题目】下列说法,不正确的是( )
A.双键、三键中都含有π键
B.成键原子间原子轨道重叠愈多,共价键愈牢固
C.因每个原子未成对的电子数是一定的,故与其配对的原子个数也一定
D.所有原子轨道在空间中都有自己的方向性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( )
A.4Fe(0H)2+O2+2H2O═4Fe(OH)3
B.2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
C.3CO+Fe2O3 ![]() 3CO2+2Fe
3CO2+2Fe
D.Zn+H2SO4═ZnSO4+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然无法直接测得,但可通过间接的方法测定.现根据下列的3个热化学反应方程式:
Fe203(s)+3CO(g)=2Fe(s)+3C02(g)△H=﹣24.8kJ/mol
Fe203(s)+ ![]() CO(g)═
CO(g)═ ![]() Fe3O4(s)+C02(g)△H=﹣15.73kJ/mol
Fe3O4(s)+C02(g)△H=﹣15.73kJ/mol
Fe304(s)+CO(g)═3FeO(s)+C02(g)△H=+640.4kJ/mol
试写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列条件一定能使反应速率加快的是
①增加反应物的物质的量②升高温度③缩小反应容器的体积④加入生成物⑤加入MnO2
A. 全部B. ①②⑤C. ②D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物在工业上有许多用途.以铁硼矿(主要成分为Mg2B2O5H2O,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示: 
已知:Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、4.9、9.7和12.4.
回答下列问题:
(1)为提高“浸出”速率,除适当增加硫酸浓度外,还可采取的措施有;
(2)实验室中过滤操作所需要的玻璃仪器有:玻璃棒、;
(3)“浸渣”中的物质是(化学式);
(4)“净化除杂”需先加H2O2溶液,作用是 , 然后再调节溶液的pH约为5,目的是;
(5)“粗硼酸”中的主要杂质是(填名称);
(6)单质硼可用于生产具有优良抗冲击性能的硼钢.以硼酸和金属镁为原料在加热条件下可制备单质硼, 用化学方程式表示制备过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A和气体甲、乙、丙及物质B、C、D、E、F、G,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出).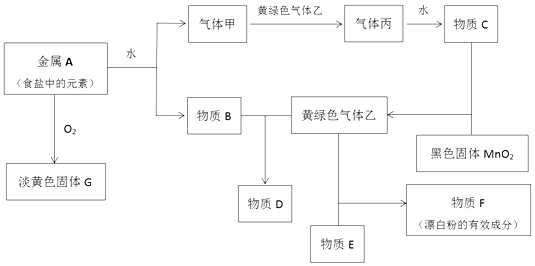
请根据以上信息回答下列问题:
(1)实验室制取氯气的化学方程式为4HCl(浓)+MnO2 ![]() Cl2↑+MnCl2+2H2O,
Cl2↑+MnCl2+2H2O,
MnO2 做剂,如果反应产生的气体在标况下体积为2.24L,则被氧化的HCl的物质的量是mol
(2)写出下列反应的离子方程式:
①金属A和水
②物质B和气体乙
(3)用两个化学方程式表示固体G可做呼吸系统供氧剂原因
(4)用化学方程式解释F长期放置在空气中失效的原因:
(5)红热细铁丝能在气体乙剧烈燃烧,现象是将燃烧产物配成饱和溶液滴入沸水中可以得到的氢氧化铁胶体,该氢氧化铁胶体粒子直径在
之间.向氢氧化铁胶体中滴入过量稀硫酸,现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是关于反应A2(g)+3B2(g)2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( ) 
A.升高温度,同时加压
B.降低温度,同时减压
C.增大反应物浓度,同时减小生成物浓度
D.增大反应物浓度,同时使用催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com