
在50 mL a mol·L-1的硝酸溶液中,加入6.4g Cu,全部溶解,假设硝酸的还原产物只有NO2和NO,将反应后溶液用蒸馏水稀释至100 mL时测得c(NO3-)=3 mol·L-1。
(1)求稀释后的溶液中H+的物质的量浓度
(2)若a=9,求生成的气体中NO2的物质的量
(3)治理氮氧化物污染的方法之一是用NaOH溶液进行吸收,反应原理如下:
NO2+NO+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO2+NaNO3+H2O。若将上述的NO2和NO的混合气体通入1 mol·L-1的NaOH溶液恰好被吸收,求需要NaOH溶液的体积。
(1)1mol/L (2)0.125 mol (3) 150ml
【解析】
试题分析:(1)6.4g Cu的物质的量为6.4g÷64g/mol=0.1mol,所以溶液n(Cu2+)=n(Cu)=0.1mol,溶液中c(NO3-)=c(H+)+2c(Cu2+),因此溶液中c(H+)=2c(Cu2+)-c(NO3-)=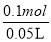 ×2-3mol/L=1mol/L。
×2-3mol/L=1mol/L。
(2)根据N元素守恒,可知n(NO2)+n(NO)=n硝酸溶液(HNO3)-n反应后溶液(NO3-)=0.05L×9mol/L=0.45mol-0.1L×3mol/L=0.15mol,令NO2、NO的物质的量分别为xmol、ymol,则:x+y=0.15、x+3y=0.1×2,解得,x=0.125,y=0.025。
(3)反应后为NaNO2、NaNO3混合溶液,根据N元素守恒可知,n(NaNO2)+n(NaNO3)=n(NO2)+n(NO)=0.15mol,根据钠元素守恒可知,n(NaOH)=n(NaNO2)+n(NaNO3)=0.15mol,NaOH溶液的体积为0.15mol÷1L/mol=0.15L=150mL。
考点:考查硝酸的性质以及氧化还原反应的有关计算


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源:2016届山东省高一上学期期中考试化学试卷(解析版) 题型:填空题
实验室中所用少量氯气是用下列方法制取的:
4HCl(浓)+MnO2 Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O
(1)该反应既是离子反应也是氧化还原反应。该反应的还原剂是 (用化学式表示)。
氯气有毒会污染空气,实验室常用氢氧化钠吸收该实验的尾气,写出用氢氧化钠溶液吸收氯气的离子方程式 。
(2)若有17.4gMnO2与足量的浓盐酸充分反应后, 所得溶液的体积为500 mL,求:
①转移电子数为______ _;
②被氧化的HCl的物质的量_______ mol;
查看答案和解析>>
科目:高中化学 来源:2016届山东省威海市高一上学期期末考试化学试卷(解析版) 题型:选择题
将一小块金属钠投入足量的下列溶液中,既能生成气体,又能生成蓝色沉淀的是
A.CuSO4溶液 B.Ba(OH)2稀溶液
C.MgCl2溶液 D.CaCl2溶液
查看答案和解析>>
科目:高中化学 来源:2016届天津市五区县高一上学期期末考试化学试卷(解析版) 题型:选择题
N0为阿伏加德罗常数的值,下列叙述正确的是
A.1 mol CO2中含有原子数N0
B.1 L 1mol/L的硫酸钠溶液中,所含Na+数为N0
C.标准状况下,11.2 L水所含分子数为0.5 N0
D.在反应中,1 mol Fe和足量盐酸反应失去的电子数为2 N0
查看答案和解析>>
科目:高中化学 来源:2016届天津市五区县高一上学期期末考试化学试卷(解析版) 题型:选择题
20mL 1mol ·L_1NaOH与1mol ·L_1的硫酸反应,溶液呈中性,则硫酸的体积为 ( )
A.5 mL B.l0 mL
C.20 mL D.40 mL
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高一教学评估(一)化学试卷(解析版) 题型:选择题
将一定量的锌与100mL18.5mol/L浓硫酸充分反应后,锌完全溶解,同时生成气体A 33.6L(标准状况).将反应后的溶液稀释至1L,测得溶液的c(H+)=0.1mol·L-1,则下列叙述中错误的是
A.气体A为SO2和H2的混合物
B.气体A中SO2和H2的体积比为4:1
C.反应中共消耗Zn 97.5g
D.反应中共转移3mol电子
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高一教学评估(一)化学试卷(解析版) 题型:选择题
下列关于二氧化硫性质的说法正确的是
A.氯水中通入一定量二氧化硫气体可增强氯水的漂白性
B.含有酚酞的氢氧化钠溶液中通入二氧化硫气体,溶液变无色,说明二氧化硫具有漂白性
C.二氧化硫既可被氧化也可被还原
D.紫色石蕊试液中通入二氧化硫,溶液先变红后退色
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高一上学期期末质量检测化学试卷(解析版) 题型:选择题
甲、乙两烧杯中分别盛有100mL 3.0mol·L—1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成气体体积比:甲∶乙=1∶2,则加入铝粉的质量为
A. 5.4g B. 3.6g C. 2.7g D. 1.8g
查看答案和解析>>
科目:高中化学 来源:2015届福建省龙岩市高二第一学期教学质量检测化学试卷(解析版) 题型:填空题
现有常温下的0.1 mol/l纯碱溶液。
(1)该溶液呈碱性是因为存在水解平衡,相关离子方程式是:________________。为证明存在上述平衡,进行如下实验:在0.1 mol·l-1纯碱溶液中滴加酚酞,溶液显红色,再往溶液中滴加 (填化学式)溶液,红色逐渐退为无色,说明上述观点成立。
(2)同学甲查阅资料得知0.1 mol/LNa2CO3中,发生水解的CO32—不超过其总量的10%。请设计实验加以证明(写出实验方案及预期观察到的现象)。答: 。
(3)同学乙就该溶液中粒子浓度关系写出五个关系式,其中不正确的是 。
A.c(Na+)>2c(CO32—)
B.c(CO32—)>c(OH-)>c(HCO3—)>c(H2CO3)
C.c(OH-)=c(H+)+c(HCO3—)+2c(H2CO3)
D.c(CO32—)+c(HCO3—)=0.1 mol·L-1
E.c(H+)+ c(Na+)= c(OH-)+c(HCO3—)+c(CO32—)
(4)室温下pH均为a的Na2CO3和NaOH溶液中,水电离产生的c(OH—)之比= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com