
【题目】《本草纲目》中的“石碱”条目下写道:“采蒿蓼之属……晒干烧灰,以原水淋汁……久则凝淀如石……浣衣发面,甚获利也。”下列说法中错误的是
A.“石碱”的主要成分易溶于水
B.“石碱”俗称烧碱
C.“石碱”可用作洗涤剂
D.“久则凝淀如石”的操作为结晶
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
【题目】砷化稼(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]_______________。
(2)根据元素周期律,元素的电负性Ga______(填“大于”或“小于”, 下同)As,第一电离能B ____ Ga;BF3和NH3的分子能够通过配位键相结合的原因是_______。
(3)杀虫剂Na3AsO4中阴离子的空问构型为______,As原子采取________杂化。
(4)组成相似的GaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是____________。
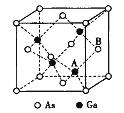
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价健数为______;A原子距离B原子所在六面体的侧面的最短距离为______ (用x表示)pm ;该晶胞的密度为_____g·cm-3。(阿伏伽德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应A(g)+3B(g)![]() 2C(g)。若维持温度和压强不变,当达到平衡时,容器的体积为VL,其中C气体的体积占10%。下列判断中正确的是 ( )
2C(g)。若维持温度和压强不变,当达到平衡时,容器的体积为VL,其中C气体的体积占10%。下列判断中正确的是 ( )
A. 原混合气体的体积为1.2VL
B. 原混合气体的体积为1.1VL
C. 反应达到平衡时气体A消耗掉0.5VL
D. 反应达到平衡时气体B消耗掉0.05VL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点.
(1)烟气脱硫、脱硝的环境意义是;
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3 ![]() 7N2+12H2O
7N2+12H2O
①上述反应中被还原的元素是(填元素符号),反应中每转移2.4mol电子,生成N2的物质的量为 .
②超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ、O3 ![]() O+O2
O+O2
Ⅱ、NO+O3→NO2+O2
Ⅲ、NO2+O→NO+O2
上述反应中NO所起的作用是 .
(3)表列出了2种燃煤烟气脱硫方法的原理.
方法Ⅰ | 用氨水将SO2转化为NH4HSO3 , 再氧化成(NH4)2SO4 |
方法Ⅱ | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫 |
方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3 , 写出该反应的离子方程式: , 是利用了SO2的性质(选填字母编号).
A.漂白性 B.氧化性 C.还原性 D.酸性氧化物.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】印刷电路板在科技领域具有不可替代的作用,它的制备方法为高分子化合物和铜箔压合,通过FeCl3溶液“腐蚀”而成。某实验小组在实验室用废弃的印刷电路板和“腐蚀液”提取铜的一种工艺流程如下:

请回答下列问题:
(1)检验“腐蚀液”中含有Fe3+的方法为_________________。
(2)“分离”所用的操作名称为____________,该操作所用的主要玻璃仪器有烧杯、_________________________。
(3)用电解法在铁上镀铜时,阴极材料为_____________(填化学式),理论上电镀过程中电解质溶液的浓度_________(填“增大”“减小”或“不变”)。
(4)Fe2+溶液有很多重要用途。
①已知:常温下,Ksp[Fe(OH)2]=1.8×10-16。保存1.8mol·L-1的FeSO4溶液时,为确保溶液中不出现浑浊,应调节溶液的pH不超过_________________。
②Fe2+转化为Fe3+后,可用于制备高铁酸盐。向FeCl3溶液中加入NaOH、NaClO溶液制备Na2FeO4的化学方程式为_________________________。
③Fe2+可使Ag+与Fe3+之间相互转化。一定温度下,0.1 mol·L-1的Fe(NO3)2溶液中,c(Fe3+)与c(Ag+)的关系如图所示:Fe2+ + Ag+![]() Fe3+ + Ag
Fe3+ + Ag

该温度下,A点溶液中转化反应的平衡常数为____________(溶液体积变化忽略不计);若将0.6mol·L-1 Fe(NO3)2溶液、0.15 mol·L-1 Fe(NO3)3溶液、0.06 mol L-1 AgNO3溶液等体积混合后,再加入1.08 g Ag,可观察到的现象为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com