
【题目】在2 L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,则此溶液中Ca2+离子的物质的量是

A. 0.5 mol B. 1.0 mol C. 2.0 mol D. 3.0 mol
科目:高中化学 来源: 题型:
【题目】下列各物质的化学式、对应的名称(或俗名)、物质所属的类别都正确的是( )
A. Fe2O3 氧化亚铁 碱性氧化物 B. CO2 二氧化碳 酸性氧化物
C. H2SO3 硫酸 酸 D. Na2CO3 纯碱 碱
查看答案和解析>>
科目:高中化学 来源: 题型:
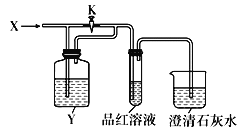
【题目】向如图所示装置中缓慢通入气体X,若打开活塞K,则品红溶液褪色;若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊。X和Y可能是
选项 | A | B | C | D |
X | SO2 | Cl2 | HCl | Cl2 |
Y | NaOH溶液 | 饱和NaHCO3溶液 | 饱和NaCl溶液 | Na2SO3溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,向2L密闭容器中加入1molNO和1mol活性炭,发生反应: ![]() H=-213.5kJ/mol,达到平衡时的数据如下:
H=-213.5kJ/mol,达到平衡时的数据如下:
温度/℃ | n(活性炭)/mol | n(CO2)/mol |
T1 | 0.70 | —— |
T2 | —— | 0.25 |
下列说法不正确的是
A. 上述信息可推知:T12
B. T1℃时,该反应的平衡常数K=9/16
C. T2℃时,若反应达平衡后再缩小容器的体积,c(N2):c(NO)不变
D. T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知淀粉酶的成分为蛋白质,可将淀粉分解为葡萄糖。分析表格,可推测( )
溶液 | 双缩脲试剂 | 碘液 | 斐林试剂 |
甲 | + | - | - |
乙 | - | ++ | - |
甲、乙混合 | + | + | + |
注:“+”显色,“++”显色更深;“-”不显色。
A. 甲溶液含有淀粉 B. 乙溶液含有还原性糖
C. 混合溶液不含淀粉 D. 混合溶液含有淀粉酶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】书写下列化学用语:
(1)氯碱工业中电解饱和食盐水总反应的离子方程式________。
(2)泡沫灭火器所用的原料为硫酸铝和碳酸氢钠,用离子方程式表示泡沫灭火器的灭火原理________。
(3)向含有Mg(OH)2固体的浊液中加入浓NH4Cl溶液,Mg(OH)2固体溶解,用化学方程式解释原因________。
(4)以甲烷、空气为燃料,以KOH为电解质溶液的燃料电池,负极反应式________,正极反应式________。
(5)用惰性电极电解溶融Al2O3可以获得活泼金属Al,写出阳极的电极反应式________,总反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管柱,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是

A. 通入保护电流使钢管桩表面腐蚀电流接近于零
B. 通电后外电路电子被强制从高硅铸铁流向钢管桩
C. 高硅铸铁的作用是作为损耗阳极材料和传递电流
D. 通入的保护电流应该根据环境条件变化进行调整
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物![]() 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物![]() 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是
A. 溶液A和B均可以是盐酸或氢氧化钠溶液
B. 溶液A和B均可以选用稀硝酸
C. 若溶液B选用氯化铁溶液,则实验难以实现
D. 实验方案Ⅱ更便于实施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1998年诺贝尔化学奖授予科恩和波普尔,以表彰他们在理论化学领域作出的重大贡献.他们的实验和理论能共同协力探讨分子体系的性质.下列说法正确的是
A.未来化学的研究方向是经验化B.化学不需要再做实验
C.化学不再是纯实验学科D.化学不做实验,就什么都不知道
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com