
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
(已知N2(g)+3H2(g) 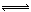 2NH3(g) ΔH=-92.4 kJ·mol-1):
2NH3(g) ΔH=-92.4 kJ·mol-1):
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1 mol N2、3 mol H2 | 2 mol NH3 | 4 mol NH3 |
| NH3的浓度 | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
下列说法正确的是
A.2c1>c3 B.a+b=92.4 C.2p2<p3 D.α1+α3>1
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物,力图使所有作为原料的原子都被产品所消纳,实现“零排放”。以下反应不符合绿色化学原子经济性要求的是
A.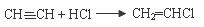 B.
B.
C.CH2=CH2 + HCl  CH3CH2Cl D.
CH3CH2Cl D.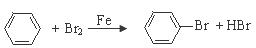
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应:2SO2+O2 2SO3的平衡状态下,保持恒温恒容,向容器中加入一定量的O2,下列说法正确的是(K为平衡常数,Qc为浓度商)
2SO3的平衡状态下,保持恒温恒容,向容器中加入一定量的O2,下列说法正确的是(K为平衡常数,Qc为浓度商)
A.Qc不变,K变大,O2转化率增大 B. Qc不变,K变大,SO2转化率减小
C. Qc变小,K不变,O2转化率减小 D. Qc增大,K不变,SO2转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述不正确的是
A.等浓度的NaCN、NaHSO3混合溶液中:c(HCN)+c(CN-)= c(HSO3-)+c(H2SO3)
B.pH= 4.5的食醋中c(H+)是pH= 6.5的番茄汁中c(H+)的100倍
C.10 ml pH=2的HA溶液、HB溶液分别与足量的锌反应,HA溶液放出的氢气较多,说明HA的酸性比HB的弱
D.pH= 4.5的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧分别进行如图所示的可逆反应,各物质的起始加入量如下:A、B和C均为4.0 mol、D为6.5 mol、F为2.0 mol,设E为x mol,当x在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器的正中位置,请填写以下空白。
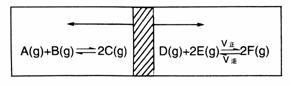
(1)若x=4.5,则右侧反应在起始时向__________(填“正反应”或“逆反应”)方向进行,要使起始反应维持向该方向进行,则x的取值范围__________。
(2)若x=4.5和5.0,则在这种情况下,当反应达平衡时,A的物质的量是否相等?__________(填“相等”、“不相等”或“不能确定”),其理由是__________________。\
查看答案和解析>>
科目:高中化学 来源: 题型:
除去粗盐中的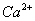 、
、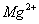 、
、 ,可先将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液。下列操作顺序正确的是
,可先将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液。下列操作顺序正确的是
A.②⑤④①③ B.⑤②①④③
C.①④②⑤③ D.④①②⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
N2、CO2、SO2三种气体的质量比为7:11:16时,它们的分子个数比为___________;物质的量之比为___________;同温同压下体积比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2===Na2S2O5。
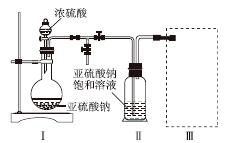
(1)装置Ⅰ中产生气体的化学方程式为______________________________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是______。
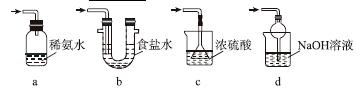
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。
实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO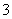 的电离程度大于水解程度,可采用的实验方法是________(填序号)。
的电离程度大于水解程度,可采用的实验方法是________(填序号)。
a.测定溶液的pH b.加入Ba(OH)2溶液
c.加入盐酸 d.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检测Na2S2O5晶体在空气中已被氧化的实验方案是
________________________________________________________________________
________________________________________________________________________。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O===H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测定结果________(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com