

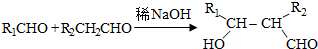
 ��
�� ��
�� ��
�� ��д�ṹ��ʽ��
��д�ṹ��ʽ�� ���� ��A����Է�������Ϊ70���˴Ź���������ʾֻ��һ�ֻ�ѧ�������⣬$\frac{70}{12}$=5��10����AΪC5H10���ṹΪ ��A����������ȡ����Ӧ����BΪ
��A����������ȡ����Ӧ����BΪ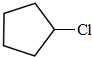 ��B������ȥ��Ӧ����CΪ
��B������ȥ��Ӧ����CΪ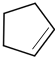 ��������C�ķ���ʽΪC5H8��C����������Ӧ����DΪHOOC��CH2��3COOH��E��FΪ��Է���������14��ͬϵ�F�Ǹ������ֵ����ʣ���FΪHCHO����֪EΪCH3CHO������Ϣ�ܿ�֪E��F��Ӧ����GΪOHCH2CH2CHO��G�����������ӳɷ�Ӧ����HΪOHCH2CH2CH2OH��D��H�������۷�Ӧ����PPG��
��������C�ķ���ʽΪC5H8��C����������Ӧ����DΪHOOC��CH2��3COOH��E��FΪ��Է���������14��ͬϵ�F�Ǹ������ֵ����ʣ���FΪHCHO����֪EΪCH3CHO������Ϣ�ܿ�֪E��F��Ӧ����GΪOHCH2CH2CHO��G�����������ӳɷ�Ӧ����HΪOHCH2CH2CH2OH��D��H�������۷�Ӧ����PPG��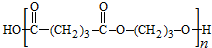 �����ݴ˷������
�����ݴ˷������
��� �⣺��A����Է�������Ϊ70���˴Ź���������ʾֻ��һ�ֻ�ѧ�������⣬$\frac{70}{12}$=5��10����AΪC5H10���ṹΪ ��A����������ȡ����Ӧ����BΪ
��A����������ȡ����Ӧ����BΪ ��B������ȥ��Ӧ����CΪ
��B������ȥ��Ӧ����CΪ ��������C�ķ���ʽΪC5H8��C����������Ӧ����DΪHOOC��CH2��3COOH��E��FΪ��Է���������14��ͬϵ�F�Ǹ������ֵ����ʣ���FΪHCHO����֪EΪCH3CHO������Ϣ�ܿ�֪E��F��Ӧ����GΪOHCH2CH2CHO��G�����������ӳɷ�Ӧ����HΪOHCH2CH2CH2OH��D��H�������۷�Ӧ����PPG��
��������C�ķ���ʽΪC5H8��C����������Ӧ����DΪHOOC��CH2��3COOH��E��FΪ��Է���������14��ͬϵ�F�Ǹ������ֵ����ʣ���FΪHCHO����֪EΪCH3CHO������Ϣ�ܿ�֪E��F��Ӧ����GΪOHCH2CH2CHO��G�����������ӳɷ�Ӧ����HΪOHCH2CH2CH2OH��D��H�������۷�Ӧ����PPG��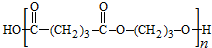 ����
����
��1��ͨ�����Ϸ���֪��A�Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2��BΪ ��B������ȥ��Ӧ����CΪ
��B������ȥ��Ӧ����CΪ ����Ӧ����ʽΪ�ʴ�Ϊ��
����Ӧ����ʽΪ�ʴ�Ϊ�� ��
��
��2����B����C�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��3����E��F����G�ķ�Ӧ����Ϊ�ӳɷ�Ӧ���ʴ�Ϊ���ӳɷ�Ӧ��
��4����D��H����PPG�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��5��D��ͬ���칹������ͬʱ��������뱥��NaHCO3��Һ��Ӧ�������壬��-COOH���ڼ��ܷ���������Ӧ�����ܷ���������Ӧ��˵������-COOCH���˴Ź���������ʾΪ3��壬�ҷ������Ϊ6��1��1���� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬��ȷ�ж�A�Ľṹ��ʽ�ǽⱾ��ؼ����ٽ�Ϸ�Ӧ�����������Ϣ�����ƶϣ����ؿ���ѧ���Գ��������ż������ʡ�������Ӧ���͵�������Ӧ�ã��ѵ��ǣ�5����ṹ��ʽȷ������Ŀ�Ѷ��еȣ�


 һ��һ����ʱ���ϵ�д�
һ��һ����ʱ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ����д��BԪ�صĵ���������������Һ��Ӧ�����ӷ���ʽ2Al+2OH-+2H2O=2AlO2-+3H2����
����д��BԪ�صĵ���������������Һ��Ӧ�����ӷ���ʽ2Al+2OH-+2H2O=2AlO2-+3H2�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
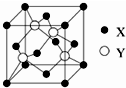 Ԫ��X λ�ڵ������ڣ����̬ԭ�ӵ��ڲ���ȫ���������ӣ�������������Ϊ2��Ԫ��Y��̬ԭ�ӵ�3p �������4�����ӣ�Ԫ��Z ��ԭ�����������������ڲ��3����
Ԫ��X λ�ڵ������ڣ����̬ԭ�ӵ��ڲ���ȫ���������ӣ�������������Ϊ2��Ԫ��Y��̬ԭ�ӵ�3p �������4�����ӣ�Ԫ��Z ��ԭ�����������������ڲ��3�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
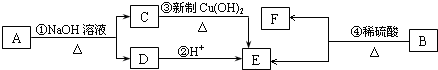
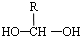 $\stackrel{-H_{2}O}{��}$
$\stackrel{-H_{2}O}{��}$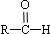 ��R������������
��R������������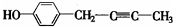 ��
��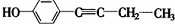 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
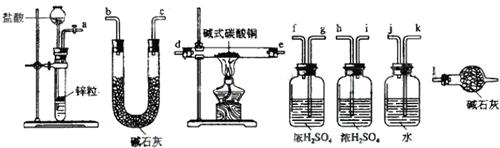
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��д�ṹ��ʽ��
��д�ṹ��ʽ�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2�� | B�� | 3�� | C�� | 4�� | D�� | 5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.6mol H2SO4 | B�� | 3.612��1023��HNO3���� | ||
| C�� | 7.3g HCl | D�� | 4.48L CH4 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com