
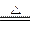 2NaOH+2Na2CO3+O2��
2NaOH+2Na2CO3+O2��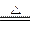 4Na2CO3+O2��+2H2O
4Na2CO3+O2��+2H2O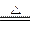 Na2CO3+CO2��+H2O
Na2CO3+CO2��+H2O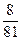 m
m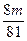 <��m��
<��m��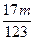
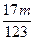 <��m<
<��m<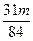
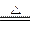 2NaOH+2Na2CO3+O2��
2NaOH+2Na2CO3+O2��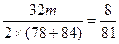 m
m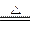 4Na2CO3+O2��+2H2O
4Na2CO3+O2��+2H2O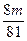 <��m��
<��m��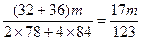
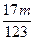 <��m<
<��m<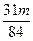 ��
��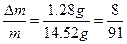 ����a/b<1�������Na2O2��������m=m(O2)��n(O2)=
����a/b<1�������Na2O2��������m=m(O2)��n(O2)=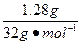 ="0.04" mol��
="0.04" mol��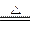 2NaOH + 2Na2CO3+O2��
2NaOH + 2Na2CO3+O2��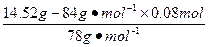 ="0.1" mol
="0.1" mol


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������6.2�� | B������6.2�� |
| C����6.2�� | D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��H2 | B��CO | C��C12H22O11 | D��C6H12O6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
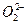 �Ĺ���������������в���ȷ����( )
�Ĺ���������������в���ȷ����( )| A�����������Ļ�ѧʽ��BaO2 |
B��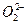 �ĵ���ʽ�ǣ� �ĵ���ʽ�ǣ� ��2- ��2- |
| C��1 mol Na2O2��BaO2��������ˮ��Ӧ������0.5 mol O2 |
| D���������ƺ�����������ǿ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������Ͷ��ˮ�� | B�����ȵ�����ˮ������Ӧ |
| C����������Ͷ��ˮ�� | D�����ȵ�ľ̿������Ũ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��9.2g | B��2.3g | C��1.84g | D��0.92g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaOH | B��Na2O | C��Na2O2 | D��NaHCO3 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com