
| A. | 锌铁 | B. | 铁铝 | C. | 铁铜 | D. | 不能确定 |
分析 某合金2.25克与足量稀硝酸反应得到标准状况下的气体1.12升,气体物质的量n=$\frac{1.12L}{22.4L/mol}$=0.05mol,转移电子总数为0.05mol×(5-2)=0.15mol,则合金金属的平均摩尔质量=$\frac{2.25g}{0.15mol}$=15g/mol,据此计算各组金属的平均摩尔电子质量比较分析判断.
解答 解:某合金2.25克与足量稀硝酸反应得到标准状况下的气体1.12升,气体物质的量n=$\frac{1.12L}{22.4L/mol}$=0.05mol,转移电子总数为0.05mol×(5-2)=0.15mol,则合金金属的平均摩尔质量=$\frac{2.25g}{0.15mol}$=15g/mol,
A.Zn的电子摩尔质量=$\frac{65}{2}$=32.5g/mol,Fe的摩尔电子质量=$\frac{56}{3}$=18.7g/mol,二者不可以平均到15g/mol,故A错误;
B.Fe的摩尔电子质量=$\frac{56}{3}$=18.7g/mol,Al的摩尔电子质量=$\frac{27}{3}$=9g/mol,二者可以平均到15g/mol,故B正确;
C.Fe的摩尔电子质量=$\frac{56}{3}$=18.7g/mol,Cu的摩尔电子质量=$\frac{64}{2}$32g/mol,二者不可以平均到15g/mol,故C错误;
D.上述分析可知能确定,故D错误;
故选B.
点评 本题考查了金属和酸反应过程中电子守恒的计算,主要是平均摩尔电子质量的计算应用,掌握基础是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
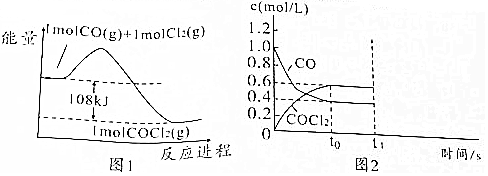
 ;光气遇水后生成两种气体,其中一种气体极易溶于水,反应的化学方程式为COCl2+H2O═2HCl+CO2;
;光气遇水后生成两种气体,其中一种气体极易溶于水,反应的化学方程式为COCl2+H2O═2HCl+CO2;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 电化学与我们的生活有着密切的联系,请结合电化学知识回答下列有关问题.
电化学与我们的生活有着密切的联系,请结合电化学知识回答下列有关问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某化学兴趣小组设置了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质,下列说法不正确的是( )
某化学兴趣小组设置了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质,下列说法不正确的是( )| A. | 利用I、II装置制取气体(K2关闭、K1打开),可以在II中收集H2等气体,但不能收集HCl气体 | |
| B. | 若装置II中装满水后,可以收集O2、NO等气体,但不能收集NO2、CO2等气体 | |
| C. | 利用I、Ⅲ装置(K1关闭、K2打开,A中装硝酸)可以比较N、C、Si元素非金属性强弱 | |
| D. | 若在Ⅲ装置的小试管C中加入一定量CCl4和AgNO3溶液(导管伸入CCl4层),则利用I、Ⅲ装置(K1关闭、K2打开)可验证苯与液溴发生的是取代反应,不是加成反应 |
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第三次月考化学试卷(解析版) 题型:推断题
1,4- 二苯基丁烷是用来研究聚合物溶剂体系热力学性质的重要物质,工业上用下列方法制备1,4-二苯基丁烷:
友情提示:格拉泽反应:2R—C≡C—H  R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2

回答下列问题:
(1)D的官能团的名称为 。
(2)①和③的反应类型分别为 、 。
(3)E的结构简式为 。用1 mol E合成1,4-二苯基丁烷,理论上需要消耗氢气_______mol。
(4)请写出反应①的化学方程式____________________________。
(5)化合物C在氢氧化钠的水溶液中加热可得到化合物F,请写出化合物F和乙酸反应的化学方程式___________________。
(6)芳香化合物G是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为1:1,写出其结构简式______________________。
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | 浓硝酸和稀硝酸都具有强氧化性 | 浓硝酸和稀硝酸均可使紫色石蕊试液先变红后褪色 |
B | 浓硫酸具有强氧化性和吸水性 | 浓硫酸可干燥H2和CO,不可干燥 SO2和NH3 |
C | SO2是酸性氧化物 | SO2可使含有酚酞的NaOH溶液褪色 |
D | 铵盐受热易分解 | NH4Cl和NH4HCO3均可用作氮肥和制取氨气 |
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古高三上月考二化学试卷(解析版) 题型:选择题
下列反应中,水作为还原剂的是
A.Cl2+H2O=HCl+HClO
B.2Na2O2+2H2O=4NaOH+O2
C.2F2+2H2O=4HF+O2
D.2Na+2H2O=2NaOH+H2
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
分类是化学学习与研究的常用方法,下列分类正确的是( )
A.C l2O7、P2O5、SO3、CO2均属于酸性氧化物
l2O7、P2O5、SO3、CO2均属于酸性氧化物
B.Na2O、Na2O2为相同元素组成的金属氧化物,都属于碱性氧化物
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com