���𰸡�
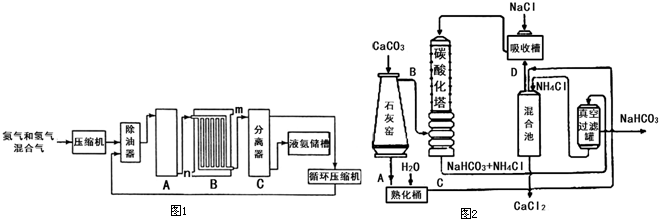
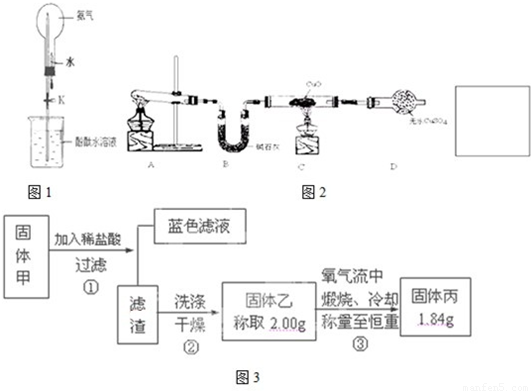
��������1��ʵ�������Ȼ�狀��������Ƽ�����ȡ������
��2���ٰ����Ǽ�������ˮ�����壬��������ˮ����ƿ��ѹǿ���٣�����ѹǿ�������Һ������ƿ��
�ڰ���������ˮ����һˮ�ϰ���һˮ�ϰ�����������ʣ���������������ӣ�
��3���ٸ���ʵ�������ж������
�ڼ�ʯ���Ǹ������
�۸��ݰ��������ʷ����жϣ���ֹ��Ⱦ������
��ͭ��������ᷴӦ����Ӧ����Һ�е����������������ͭ������������NO
3-��H
+������ͭ��NO
3-��Cu
2+�Ĺ�ϵʽ��⣻
�ڸ��ݵ����غ�͵�Ԫ���غ���⣻
��1���۸������ʵ����ʺ������仯�ĽǶ�֪��Ӧ��
��2���������ϡ����õ�����ɫ��Һ��˵������ijɷ���CuO��Cu
2O������һ�֣�
������Ӧ��Cu+O
2
CuO ���أ�Cu
2S+2O
2
2CuO+2SO
2 ���䣻2CuS+3O
2
2CuO+2SO
2 ���أ�������������ҳ�ȡ2.00g�������������ա���ȴ���������أ��ù����1.84g������ʵ�ʱ����ˣ�˵������CuS�������������ʣ�
����⣺��1���ڼ��������£��Ȼ�狀��������Ʒ�Ӧ�����Ȼ��ơ�������ˮ��
�ʴ�Ϊ��2NH
4Cl+Ca��OH��
2 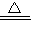
CaCl
2+2NH
3��+2H
2O��
��2����NH
3�����ܽ���ˮ��1���ˮ�ܽ�700�����������ֹˮ�м�����ͷ�ι��е�ˮ��Ȼ���ֹˮ��K�����ڰ���Ѹ���ܽ��ڼ�����ͷ�ι��е�ˮ��������ƿ������ѹǿѸ�ټ�С��������Һ������ƿ������Ȫ����
�ʴ�Ϊ�����ἷѹ�ιܣ�ʹ����ˮ������ƿ��Ȼ���ֹˮ��K��
�ڰ�����ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ������笠����Ӻ����������ӣ��������뵼����Һ�ʼ��ԣ���̪��Һ������ɫ��
�ʴ�Ϊ��NH
3+H
2O?NH
3?H
2O?NH
4++OH
-��
��3���ٺ�ɫCuO��Ϊ��ɫ����ɫ��ͭ��������������ͭ����ɫ��ˮCuSO
4��ĩ��Ϊ��ɫ������ˮ������ͭ��˵�������ﺬ��ˮ��ͬʱ����һ����ɫ���壬����������Ⱦ�����Ը������ǵ�����
�ʴ�Ϊ��3CuO+2NH
3 
3Cu+N
2+3H
2O��
�ڼ�ʯ���Ǹ������������ˮ��������ֹ���Ų���ˮ�IJⶨ���ʴ�Ϊ�����հ����л��е�ˮ��������ֹ���Ų���ˮ�IJⶨ��
�۰����Ǵ̼������壬���Բ������������Ӧ��β������װ�ã�������������ˮ���ʴ�Ϊ������һ�����հ���װ�ã���ͼ��ʾ��
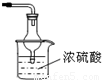
��
��
��3.2gCu�����ʵ�����n��Cu��=3.2g÷64g/mol=0.05mol��
Cu��NO
3��
2 =Cu
2++2NO
3-��HNO
3�TH
++NO
3- 0.05mol 0.1mol amol amol
���ʱ��Һ�к���NO
3-�����ʵ���Ϊ��0.1+a ��mol��
��Ũ������ͭ��Ӧ����NO
2�����ŷ�Ӧ�Ľ��У������Ũ�����ͣ�������NO����Ӧ����Һ�����������n��NO
3-��=0.1+amol��30mL��8mol/L����HNO
3��Ӧ��n��HNO
3��=0.24mol������������NOΪxmol��NO
2Ϊymol��
��NԪ���غ��֪��x+y=0.24-��0.1+a�������ݵ����غ�ɵã�3x+y=2×0.05
��֮�ã�x=��0.02-0.5a��mol��
�ʴ�Ϊ����0.02-0.5a��×22.4L��
��
��1���۸��ݷ�Ӧ�жϣ�Cu+O
2
CuO ���أ�Cu
2S+2O
2
2CuO+2SO
2 ���䣻2CuS+3O
2
2CuO+2SO
2 ���أ���һ����2CuS+3O
2
2CuO+2SO
2���ʴ�Ϊ��2CuS+3O
2
2CuO+2SO
2��
��2���������ϡ����õ�����ɫ��Һ��˵������ijɷ���CuO��Cu
2O������һ�֣�
������������ҳ�ȡ2.00g�������������ա���ȴ���������أ��ù����1.84g������ʵ�ʱ����ˣ�˵������CuS����Ҫ���������ʣ����ۣ�������Cu
2O��Cu
2S���п��ޣ�������Cu
2O������Cu
2S�������Ϸ��������ڹ���ijɷֵ��ж��У���ȷ����BCD���ʴ�Ϊ��BCD��
���������⿼���˰��������ʺ���ȡ��������������ԭ��Ӧ�ļ��㣬������ͭ��������ʣ��ѶȽϴ��ۺ���ǿ���������������ʵ����Ƶ���Ϣ���˽��ԭ��������������ԭ��Ӧ�ļ��㣬ע��������غ㡢����غ�ĽǶȽ����⣮

 CuO ���أ�Cu2S+2O2
CuO ���أ�Cu2S+2O2 2CuO+2SO2 ���䣻2CuS+3O2
2CuO+2SO2 ���䣻2CuS+3O2 2CuO+2SO2 ���أ�������������ҳ�ȡ2.00g�������������ա���ȴ���������أ��ù����1.84g������ʵ�ʱ����ˣ�˵������CuS�������������ʣ�
2CuO+2SO2 ���أ�������������ҳ�ȡ2.00g�������������ա���ȴ���������أ��ù����1.84g������ʵ�ʱ����ˣ�˵������CuS�������������ʣ�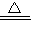 CaCl2+2NH3��+2H2O��
CaCl2+2NH3��+2H2O��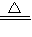 3Cu+N2+3H2O��
3Cu+N2+3H2O��  ��
�� CuO ���أ�Cu2S+2O2
CuO ���أ�Cu2S+2O2 2CuO+2SO2 ���䣻2CuS+3O2
2CuO+2SO2 ���䣻2CuS+3O2 2CuO+2SO2 ���أ���һ����2CuS+3O2
2CuO+2SO2 ���أ���һ����2CuS+3O2 2CuO+2SO2���ʴ�Ϊ��2CuS+3O2
2CuO+2SO2���ʴ�Ϊ��2CuS+3O2 2CuO+2SO2��
2CuO+2SO2��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�