
| t/min | n (CO)/mol | n (Cl2)/mol |
| 0 | 1.20 | 0.60 |
| 1 | 0.90 | |
| 2 | 0.80 | |
| 4 | 0.20 |

分析 (1)由表中数据,可知0~2min内△n(CO)=1.2mol-0.8mol=0.4mol,由方程式可知△c(COCl2)=△c(CO)=0.4mol,再根据v=$\frac{△c}{△t}$计算v(COCl2);
(2)4min内,反应的氯气为0.6mol-0.2mol=0.4mol,由方程式可知参加反应的CO为0.4mol,故4min时CO为1.2mol-0.4mol=0.8mol,与2min时CO的物质的量相等,则2min、4min处于平衡状态;
由方程式可知,平衡时生成COCl2为0.4mol,平衡常数K=$\frac{c(COC{l}_{2})}{c(CO)×c(C{l}_{2})}$;
(3)n(COCl2)随时间的变化增大,开始为0,2min时到达平衡,平衡时COCl2为0.4mol;
(4)正反应为气体体积减小的反应,增大压强平衡正向移动,CO转化率增大,而图中随X增大时,CO的平衡转化率降低,平衡逆向移动,则X为温度,正反应为放热反应.
解答 解:(1)由表中数据,可知0~2min内△n(CO)=1.2mol-0.8mol=0.4mol,由方程式可知△c(COCl2)=△c(CO)=0.4mol,则v(COCl2)=$\frac{\frac{0.4mol}{2L}}{2min}$0.1mol/(L.min),故答案为:0.1;
(2)4min内,反应的氯气为0.6mol-0.2mol=0.4mol,由方程式可知参加反应的CO为0.4mol,故4min时CO为1.2mol-0.4mol=0.8mol,与2min时CO的物质的量相等,则2min、4min处于平衡状态,在2min~4min间,v(Cl2)正 =v(Cl2)逆,
由方程式可知,平衡时生成COCl2为0.4mol,该温度下平衡常数K=$\frac{c(COC{l}_{2})}{c(CO)×c(C{l}_{2})}$=$\frac{\frac{0.4}{2}}{\frac{0.8}{2}×\frac{0.2}{2}}$=5,
故答案为:=;5;
(3)随时间的变化,COCl2的物质的量增大,开始为0,2min时到达平衡,平衡时COCl2为0.4mol,0~4min末n(COCl2)随时间的变化示意图为: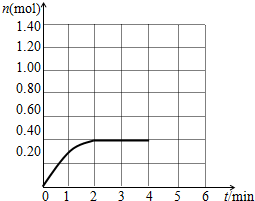 ,
,
故答案为: ;
;
(4)正反应为气体体积减小的反应,增大压强平衡正向移动,CO转化率增大,而图中随X增大时,CO的平衡转化率降低,平衡逆向移动,则X为温度,正反应为放热反应,故a<0,
故答案为:温度;<;因为X增大时,CO的平衡转化率降低,平衡逆向移动.
点评 本题考查化学平衡计算与影响因素、反应速率、平衡常数、化学平衡图象等,注意对基础知识的理解掌握.


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 L H2O所含的电子数为5NA | |
| B. | 0.1molFe原子变成 Fe3+时失去的电子数为O.3NA | |
| C. | 常温常压下,16gO2与16gO3含有的分子数为相同 | |
| D. | 0.1mol/LK2SO4溶液中含有K+数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使甲基橙呈红色的溶液:Na+、NH4+、AlO2-、CO32- | |
| B. | 8% H2O2溶液:H+、Fe2+、SO42-、Cl- | |
| C. | 含有Fe3+的溶液:Na+、Al3+、Cl-、SCN- | |
| D. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1 mol•L-1的溶液:Na+、K+、CO32-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ③④⑤ | D. | ①②②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(5x-2y)kJ•mol-1 | |
| B. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(5y-2x) kJ•mol-1 | |
| C. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(3x-y) kJ•mol-1 | |
| D. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2x-y)kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com