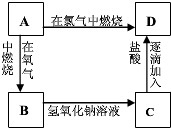
氨既是实验室中常用试剂,也是工业上重要原料.
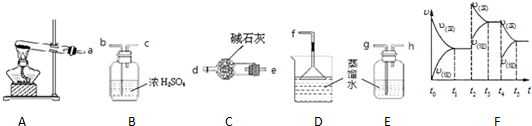
(1)某学习小组欲制备少量的氨水.供选用的试剂有:①NH
4Cl ②(NH
4)
2CO
3.提供的装置如下,请回答下列问题:
①装置A试管内发生反应的化学方程式为
;
②从提供的仪器中选择并组装一套本实验的合理、简洁装置,按气流方向连接顺序为(用图中标注的导管口符号表示)a→
;
(2)氨在氧气中燃烧,生成水和一种单质.
已知:N
2(g)+3H
2(g)?2NH
3(g)△H=-92.4kJ?mol
-12H
2(g)+O
2(g)═2H
2O(l)△H=-572kJ?mol
-1写出氨在氧气中燃烧生成液态水和气态单质的热化学方程式:
;
(3)已知在一定条件下,将1mol N
2和3mol H
2混合于一个10L的密闭容器中发生的反应为N
2+3H
22NH
3,5min后达到平衡,平衡时氨的体积分数为25%.
①该反应的平衡常数表达式K=
;
②从反应开始到平衡时,N
2的反应速率v(N
2)=
;
(4)工业上以氨气、空气为主要原料制取硝酸.在容积恒定的密闭容器中进行反应2NO(g)+O
2(g)?2NO
2(g)△H>0.该反应的反应速率(v)随时间(t)变化的关系如图F所示.若t
2、t
4时刻只改变一个条件,下列说法正确的是(填选项序号)
.
A.在t
1-t
2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
B.在t
2时,采取的措施可以是升高温度
C.在t
3-t
4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
D.在t
5时,容器内NO
2的体积分数是整个过程中的最大值
(5)为检验氨气与酸反应得到的某种常见氮肥的成分,某同学进行了以下实验:①加热氮肥样品产生气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊.②取少量该氮肥样品溶于水,并加入少量BaCl
2溶液,没有明显变化.由此可知该氮肥的主要成分可能是
(填选项序号);
A.NH
4Cl B.(NH
4)
2CO
3 C.NH
4HCO
3 D.NH
4NO
3(6)硝酸厂常用Na
2CO
3溶液吸收处理尾气NO
2生成CO
2.若9.2g NO
2和Na
2CO
3溶液完全反应时转移电子0.1mol,则反应的离子方程式是
.

 阅读快车系列答案
阅读快车系列答案