
右下图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数之和等于B的质量数的2.5倍,B元素的原子核内质子数等于中子数,下列叙述不正确的是( )
| B | ||
| A | C |
A. A为ⅤA族元素 B. B为第二周期的元素
C. C是周期表中化学性质最活泼的非金属
D. 三种元素都为非金属元素
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
钛是20世纪50年代发展起来的一种重要的结构金属,钛合金因具有强度高、耐蚀性好、耐热性高等特点而被广泛用于各个领域。
(1)与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的元素有 (填元素符号)。
(2)[Ti(OH)2(H2O)4]2+中的化学键有 。
a.σ键 b.π键 c.离子键 d.配位键
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如下图所示。

 化合物甲的分子中采取sp2杂化方式的碳原子个数为 ,化合物乙中采取sp3杂化的原子的第一电离能由小到大的顺序为 。
化合物甲的分子中采取sp2杂化方式的碳原子个数为 ,化合物乙中采取sp3杂化的原子的第一电离能由小到大的顺序为 。
(4)有一种氮化钛晶体的晶胞如右图所示,该晶体的化学式为 ,该晶体中Ti原子周围与它距离最近且相等的N原子的个数______。
查看答案和解析>>
科目:高中化学 来源: 题型:
铍元素性质与铝元素性质相似,下列方法能证明氯化铍由共价键构成的是( )
A.溶于水加硝酸银溶液,观察是否有白色沉淀生成
B.溶于水做导电实验,观察是否导电
C.熔融状态,做导电实验,观察是否导电
D.测定氯化铍熔点
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是
A.贝采里乌斯提出了有机化学概念,维勒打破了无机物和有机物的界限,范特霍夫提出了有机化合物的三维结构。
B.同位素示踪法、比色分析法都是科学家经常使用的研究化学反应历程的手段之一。
C.降低能耗是重要的节能措施,可以通过合理设计工艺路线,优化工艺条件和研制性能优良的催化剂等来实现。
D.科学家将蛋白质的结构层次分为四级进行研究,蛋白质的二级结构主要依靠肽链中-NH-上的氢原子与羰基上的氧原子形成氢键而实现的。
查看答案和解析>>
科目:高中化学 来源: 题型:
将1.00 mol·L-1 NaOH溶液滴入20.00 mL 1.00 mol·L-1的一元酸HA溶液中,测得混合溶液的pH和温度随加入NaOH溶液体积变化曲线如图所示。
(1)计算室温时20.00 mL 1.00 mol·L-1的一元酸
HA的电离度α=________。
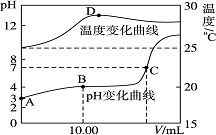 (2)图中B点所示的溶液中所含各离子浓度由
(2)图中B点所示的溶液中所含各离子浓度由
大到小的顺序是_____。
(3)下列说法正确的是________(填相应序号)。
A.由图中可知NaOH和HA反应的ΔH>0
B.图中C点所加NaOH溶液的体积V=20.00 mL
C.图中C点时溶液的KW略大于1×10-14 mol·L-1,溶液中c(H+)=1×10-7 mol·L-1
D.图中D点后,溶液温度略下降的主要原因是生成的NaA水解吸热
(4)常温下在20 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入
0.1 mol·L-1 HCl溶液40 mL,溶液中含碳元素的各种微粒
(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的
部分情况如图所示。]回答下列问题:
① 在同一溶液中,H2CO3、HCO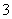 、CO
、CO
______(填“能”或“不能”)大量共存;
② 当pH=7时,溶液中含碳元素的主要微粒为________,溶液中各种离子的物质的量
浓度的大小关系为________________________________;
③ 已知在25 ℃时,CO 水解反应的平衡常数即水解常数Kh=2×10-4 mol·L-1,当溶
水解反应的平衡常数即水解常数Kh=2×10-4 mol·L-1,当溶
液中c(HCO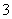 )∶c(CO
)∶c(CO )=2∶1时,溶液的pH=________。
)=2∶1时,溶液的pH=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
“3G”手机出现后,以光导纤维为基础的高速信息通道尤显重要。下列物质中用于制造光导纤维的材料是( )。
A.铜合金 B.陶瓷 C.聚乙烯 D.二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有Cl-和I-的物质的量浓度相同。为了氧化I-而不使Cl-氧化,试根据下列三个反应判断,可选用的氧化剂是( )
①2Fe3++2I-=2Fe2++I2②2Fe2++Cl2=2Fe3++2I-③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O
A.FeCl2 B.KMnO4 C.浓盐酸 D.FeCl3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com