
【题目】综合利用海水可以制备食盐、纯碱、金属镁、溴等物质,其流程如下图所示:
(1)粗盐中含有硫酸钠、氯化镁、氯化钙等可溶性杂质,为除去这些杂质而得精盐,进行如下操作:①溶解;②加过量的BaCl2溶液;③加过量的NaOH溶液;④加过量的Na2CO3溶液;⑤ ;⑥加适量的盐酸;⑦______________。(填操作名称)
(2)流程中通入的气体X为________________,理由是 。
(3)溶液Ⅱ中发生反应的化学方程式是: 。
(4)高温灼烧六水合氯化镁晶体(MgCl2·6H2O)所得固体是氧化镁,试写出该反应的化学方程式________________________________。
【答案】(1)过滤,蒸发结晶;
(2)NH3,NH3的溶解度大,有利于提高产率;
(3)NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;
(4)MgCl2·6H2O![]() MgO+2HCl↑+5H2O↑。
MgO+2HCl↑+5H2O↑。
【解析】
试题分析:(1)为了防止产生的沉淀,重现溶解,因此在加盐酸之前,应过滤;从溶液中得到NaCl固体,采用蒸发结晶的方法;(2)上述流程是制取纯碱,制取纯碱的反应方程式为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,因为氨气的极易溶于水,且溶于水后溶液显碱性,这样能更好充分利用CO2,因此先通入NH3;(3)利用碳酸氢钠的溶解需小于碳酸钠的溶解度,发生的反应是NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;(4)根据信息,反应方程式为:MgCl2·6H2O![]() MgO+ 2HCl↑+5H2O↑。
MgO+ 2HCl↑+5H2O↑。


科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)Si3N4(s)+6CO(g)
(1)该反应的氧化剂是 ,其还原产物是 ;
(2)该反应的平衡常数表达式为K= ;
(3)若知上述反应为放热反应,则其反应热△H 0(填“>”、“<”或“=”);升高温度,其平衡常数值 (填“增大”、“减小”或“不变”);若已知CO生成速率为v(CO)=18molL﹣1min﹣1,则N2消耗速率为v(N2)= ;
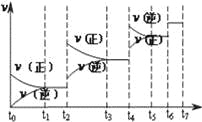
(4)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与时间t的关系如图.图中t4时引起平衡移动的条件可能是 ;图中表示平衡混合物中CO的含量最高的一段时间是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用洗净的废铜屑作原料来制备硝酸铜.下列设计路线符合“绿色化学”思想的是( )
A.Cu+HNO3(浓)→Cu(NO3)2
B.Cu+HNO3(稀)→Cu(NO3)2
C.Cu![]() CuO
CuO![]() Cu(NO3)2
Cu(NO3)2
D.Cu![]() CuSO4
CuSO4![]() Cu(NO3)2
Cu(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关过滤和蒸发的操作中,正确的是( )
A.过滤时,漏斗的下端管口紧靠烧杯内壁
B.为了加快过滤速度,可用玻璃棒搅动过滤器中的液体
C.当蒸发皿中的固体完全蒸干后,再停止加热
D.实验完毕后,用手直接取走蒸发皿
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列的分离方法不正确的是( )
A. 用过滤的方法除去食盐水中的泥沙
B. 用蒸馏的方法将自来水制成蒸馏水
C. 用酒精萃取碘水中的碘
D. 用分液的方法除去四氯化碳中的水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生欲配制6.0mol/L的H2SO41000mL,实验室有三种不同浓度的硫酸:①480mL 0.5mol/L 的硫酸;②150mL 25%的硫酸(ρ=1.18g/mL);③足量的18mol/L的硫酸.有三种规格的容量瓶:250mL、500mL、1000mL.老师要求把①②两种硫酸全部用完,不足的部分由③来补充.请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为 mol/L(保留1位小数).
(2)配制该硫酸溶液应选用容量瓶的规格为 mL.
(3)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整.
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18mol/L的浓硫酸 mL,沿玻璃棒倒入上述混合液中.并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D. ;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2cm 处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀.
(4)定容时俯视刻度线,会使所配溶液浓度 (填“偏大”、“偏小”或“无影响”).
(5)进行操作C前还需注意 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.检验Cl-的试剂是硝酸银和硝酸
B.检验SO42-的试剂是氯化钡和盐酸
C.检验CO32-的试剂是盐酸、澄清石灰水和氯化钙
D.向溶液中加入BaCl2溶液后生成白色沉淀,即可证明有SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究氮、氯、碘等单质及其化合物的反应有重要意义。
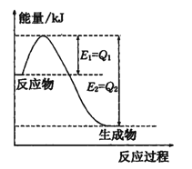
(1)如图是一定的温度和压强下N2和H2反应生成lmolNH3过程中能量变化示意图,请写出工业合成氨的热化学方程式____________(△H的数值用含字母Q1、Q2的代数式表示):
(2)已知:25℃时KSP(AgCl)=1.6×l0-10KSP(AgI)=1.5×l0-16
海水中含有大量的元素,常量元素如氯,微量元素如碘,其在海水中均以化合态存在。在25℃下,向0.1L0.002mol·L-l的NaCl溶液中逐滴加入适量的0.1L0.002mol·L-l硝酸银溶液,有白色沉淀生成,从难溶电解质的溶解平衡角度解释产生沉淀的原因是 ,向反应后的浑浊液中继续加入0.1L0.002mol·L-1的NaI溶液,看到的现象是 ,产生该现象的原因是(用离子方程式表示) 。
(3)氨气溶于水得到氨水。在25℃下,将a mol·L-1的氨水与b mol·L-1的盐酸等体积混合(混合后体积为混合前体积之和),反应后溶液显中性。求25℃下该混合溶液中氨水的电离平衡常数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将30 mL 0.5mol/L的NaOH溶液加水稀释到500 mL,稀释后NaOH的物质的量浓度为( )
A. 0.3 mol/L B. 0.05 mol/L C. 0.04 mol/L D. 0.03 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com