
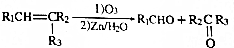
 .
.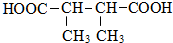 +n HOCH2CH2OH$→_{△}^{浓硫酸}$
+n HOCH2CH2OH$→_{△}^{浓硫酸}$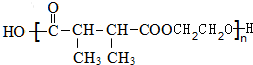 +(2n-1)H2O.
+(2n-1)H2O.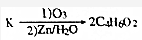 ,则K的同分异构体可能有7种(不考虑立体异构),写出其中一种的结构简式
,则K的同分异构体可能有7种(不考虑立体异构),写出其中一种的结构简式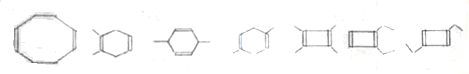 任意一种.
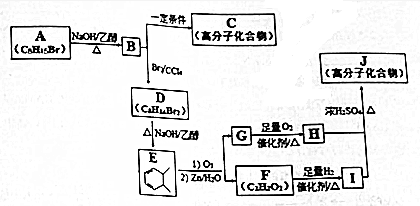
任意一种. 分析 A发生消去反应产生B,B与溴发生加成反应生成D,D再发生消去反应生成E,由E的结构、A的分子式可知A为 ,则B为
,则B为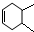 ,D为
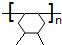
,D为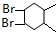 .B发生加聚反应生成C为
.B发生加聚反应生成C为 .E发生氧化反应生成F为OHC-CHO、G为
.E发生氧化反应生成F为OHC-CHO、G为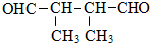 ,G氧化生成H为
,G氧化生成H为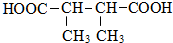 ,F与氢气发生加成反应生成I为HOCH2CH2OH,H与I发生缩聚反应生成高分子化合物J为
,F与氢气发生加成反应生成I为HOCH2CH2OH,H与I发生缩聚反应生成高分子化合物J为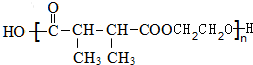 .
.
解答 解:A发生消去反应产生B,B与溴发生加成反应生成D,D再发生消去反应生成E,由E的结构、A的分子式可知A为 ,则B为
,则B为 ,D为
,D为 .B发生加聚反应生成C为
.B发生加聚反应生成C为 .E发生氧化反应生成F为OHC-CHO、G为
.E发生氧化反应生成F为OHC-CHO、G为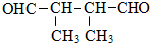 ,G氧化生成H为
,G氧化生成H为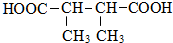 ,F与氢气发生加成反应生成I为HOCH2CH2OH,H与I发生缩聚反应生成高分子化合物J为
,F与氢气发生加成反应生成I为HOCH2CH2OH,H与I发生缩聚反应生成高分子化合物J为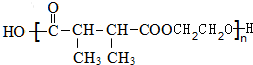 .
.
(1)B为 ,名称(系统命名)为4,5-二甲基环己烯,C的结构简式为
,名称(系统命名)为4,5-二甲基环己烯,C的结构简式为 ,
,
故答案为:4,5-二甲基环己烯; ;
;
(2)G为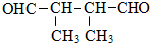 ,含有的官能团名称为醛基,A→B的反应类型为消去反应,
,含有的官能团名称为醛基,A→B的反应类型为消去反应,
故答案为:醛基;消去反应应;
(3)D为 ,含有官能团为溴原子,为检验D中的官能团,所用的试剂包括NaOH水溶液及硝酸、硝酸银溶液,
,含有官能团为溴原子,为检验D中的官能团,所用的试剂包括NaOH水溶液及硝酸、硝酸银溶液,
故答案为:硝酸、硝酸银溶液;
(4)H+I→J的化学方程式为:n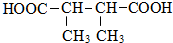 +n HOCH2CH2OH$→_{△}^{浓硫酸}$
+n HOCH2CH2OH$→_{△}^{浓硫酸}$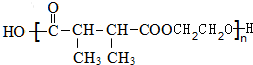 +(2n-1)H2O,
+(2n-1)H2O,
故答案为:n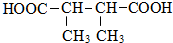 +n HOCH2CH2OH$→_{△}^{浓硫酸}$
+n HOCH2CH2OH$→_{△}^{浓硫酸}$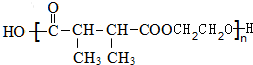 +(2n-1)H2O;
+(2n-1)H2O;
(5)E的同分异构体K能发生化学反应: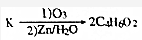 ,则K的同分异构体可能有
,则K的同分异构体可能有 ,共有7种,
,共有7种,
故答案为:7; 任意一种.
任意一种.
点评 本题考查有机物的推断,注意根据反应条件、有机物分子式与E的结构进行推断,熟练掌握官能团的性质与转化,(5)中同分异构体书写为易错点、难点.


科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10gH218O与10gD2O所含的中子数均为5NA | |
| B. | 1L0.1mol•L-1NH4Cl溶液所含NH4+数为0.1NA | |
| C. | 2.4gMg在空气中充分燃烧,转移电子数为0.2NA | |
| D. | 100g质量分数为46%的酒精水溶液中含氧原子总数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
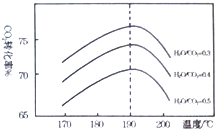 二氧化碳是一种宝贵的碳氧资源.以C02和NH3
二氧化碳是一种宝贵的碳氧资源.以C02和NH3查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 茂密树林中的道道光柱,既谁一种自然现象又是光学现象,与胶体知识无关 | |
| B. | 焰火的五彩缤纷是某些金属元素化学性质的展现 | |
| C. | “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮的氧化物无关 | |
| D. | CO2合成聚碳酸酯可降解塑料,以实现“碳”的循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
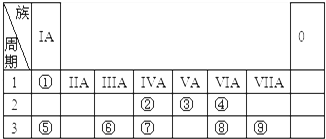
| A. | ④⑤③ | B. | ⑥①⑤③ | C. | ⑧①⑦③ | D. | ⑤②⑥③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20.625kJ | B. | 41.25kJ | C. | 82.5kJ | D. | 165.0kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 提出了元素周期律 | B. | 开发了合成氨的生产工艺 | ||
| C. | 揭示了燃烧的本质 | D. | 提取了治疟药物青蒿素 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
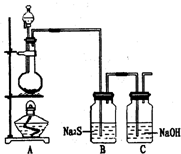 已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com