
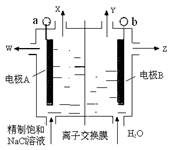
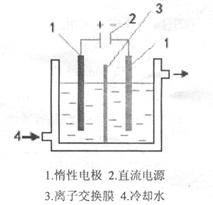
| A.精制饱和氯化钠溶液从阳极区补充 |
| B.产品烧碱溶液从阴极区流出 |
| C.产品烧碱比未用离子交换膜时更纯 |
| D.每转移NA个电子理论上可生成0.5mol 烧碱 |
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Cu2O+H2↑下列说法正确的是
Cu2O+H2↑下列说法正确的是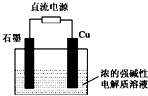
| A.石墨电极上产生氢气 |
| B.铜电极发生还原反应 |
| C.铜电极接直流电源的负极 |
| D.当有0.1mol电子转移时,有0.1molCu2O生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 沉淀完全,而在pH≥3.2时
沉淀完全,而在pH≥3.2时
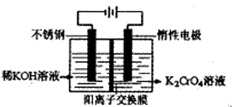
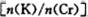 为d,则此时的铬酸钾的转化率为 。
为d,则此时的铬酸钾的转化率为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
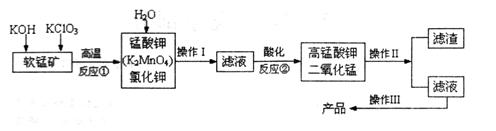
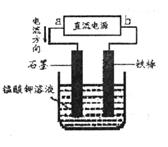
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 6Cu+SO2↑,反应的氧化剂是 。
6Cu+SO2↑,反应的氧化剂是 。
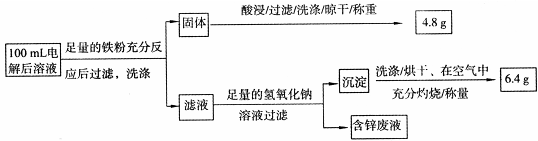
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验操作 | 现象及结论 |
| | |
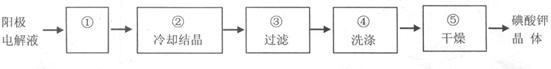
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
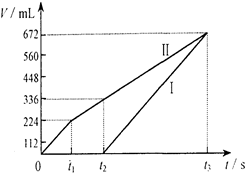
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解时以纯铜作阳极 |
| B.电解时阴极发生氧化反应 |
| C.粗铜连接电源负极,其电极反应是Cu-2e- = Cu2+ |
| D.电解后,电解槽底部会形成含少量Ag、Pt等金属的阳极泥 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com