
【题目】常温下,向浓度均为 0.1 molL-1、体积均为 100 mL 的两种一元酸 HX、HY的溶液中,分别加入 NaOH固体,lg[c(H+ )/c(OH- )]随加入 NaOH的物质的量的变化如图所示。下列说法正确的是

A. 常温下电离常数:HX < HY![]()
B. a 点由水电离出的 c(H+)=10-12 molL-1
C. c 点溶液中:c(Y- )>c(HY )![]()
D. b 点时酸碱恰好完全中和
【答案】C
【解析】A.lg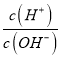 越大,溶液中氢离子浓度越大,未加NaOH时,HX溶液中lg
越大,溶液中氢离子浓度越大,未加NaOH时,HX溶液中lg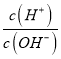 的值大,所以HX的酸性大于HY,故A错误;B.a点lg
的值大,所以HX的酸性大于HY,故A错误;B.a点lg =12,则溶液中c(H+)=0.1mol/L,溶液中水电离的c(H+)=
=12,则溶液中c(H+)=0.1mol/L,溶液中水电离的c(H+)=![]() =10-13molL-1,故B错误;C.c点lg
=10-13molL-1,故B错误;C.c点lg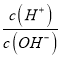 =6,则溶液中c(H+)=10-4mol/L,此时消耗的NaOH为0.005mol,则溶液中的溶质为NaY和HY,由于溶液显酸性,所以HY的电离程度大于NaY的水解程度,所以c(Y-)>c(HY),故C正确;D.浓度均为0.1molL-1、体积均100mL的HY与NaOH恰好中和消耗NaOH为0.01mol,而b点时消耗的NaOH为0.008mol,所以酸过量,故D错误;故选C。
=6,则溶液中c(H+)=10-4mol/L,此时消耗的NaOH为0.005mol,则溶液中的溶质为NaY和HY,由于溶液显酸性,所以HY的电离程度大于NaY的水解程度,所以c(Y-)>c(HY),故C正确;D.浓度均为0.1molL-1、体积均100mL的HY与NaOH恰好中和消耗NaOH为0.01mol,而b点时消耗的NaOH为0.008mol,所以酸过量,故D错误;故选C。


科目:高中化学 来源: 题型:
【题目】工业上用粗盐(含Ca2+、Mg2+、SO42-等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示。下列有关说法正确的是


A. 对粗盐溶液除杂可依次加入NaOH、Na2CO3、BaCl2,再加入盐酸调节溶液pH
B. 饱和食盐水中先通入的气体为CO2
C. 流程图中的系列操作中一定需要玻璃棒
D. 如图所示装置可以比较Na2CO3和NaHCO3晶体热稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D分别代表四种不同的元素。A原子的最外层电子排布为ns1,B原子的价电子排布为ns2np2,C原子的最外层电子数是其电子层数的3倍,D原子的L电子层的p轨道有3个电子。
(1)C原子的电子排布式为__________________,若A原子的最外层电子排布为1s1,则按原子轨道的重叠方式判断,A与C形成的化合物中的共价键类型属于______键。
(2)上述化合物A2C的熔沸点高于化合物DA3的熔沸点,其主要原因可能是____________;
(3)当n=2时,B与C形成的晶体属于 _______晶体,B与C形成的最高价化合物的结构式为_________________ 。
(4)当n=3时,B与C形成的晶体属于_______晶体,其晶体结构如下图所示。该晶体中最小的环由______个微粒构成,一个晶胞中含有______个B微粒,______个C微粒。
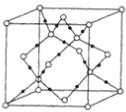
(5)若A原子的最外层电子排布为4s1,B原子的价电子排布为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序为 _______________________ (用元素符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4, Cu2O在空气中加热生成CuO
【提出假设】
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
【设计探究实验】
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则预期实验现象是_________。
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?___________。
(3)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明假设________成立,写出发生反应的所有离子方程式____________________。
【探究延伸】
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为________________。
(5)欲利用红色粉末Fe2O3和Cu2O的混合物制取较纯净的胆矾(CuSO45H2O),经查阅资料得知,在溶液中调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH
物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
开始沉淀pH | 6.0 | 7.5 | 1.4 |
沉淀完全pH | 13 | 14 | 3.7 |
实验室有下列试剂可供选择:
A.氯水 B.H2O2 C.硝酸 D.NaOH E.氨水 F.Cu2(OH)2CO3
实验小组设计如下实验方案:
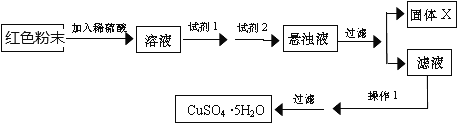
试回答:①试剂1为____________,试剂2为_____________(填字母)。
②固体X的成分为____,操作1为 ________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下发生反应:2X(g)![]() Y(g)+3Z(g) △H=akJ·mol-1(a>0)下列说法正确的是
Y(g)+3Z(g) △H=akJ·mol-1(a>0)下列说法正确的是
A. 增大X的浓度,正反应速率增大,逆反应速率减小
B. 将0.2molX充入反应器中,充分反应后,生成的Z的物质的量可能为0.09mol
C. 达到化学平衡状态时,正、逆反应的速率都为0
D. 达到化学平衡状态时,共吸收a kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2+3H22NH3合成氨反应中,在下列情况下,不能使反应速率加快的是( )
A.充入氮气
B.减小压强,扩大容器体积
C.加入催化剂
D.适当升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(NH4)2PtCl6 晶体受热分解,生成氮气、氯化氢、氯化铵和金属铂。在此分解反应中,还原产物与氧化产物的物质的量之比是( )
A.2∶3B.1∶3C.4∶3D.3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一小块金属钠投入到CuSO4溶液中,不可能观察到的现象是( )
A. 溶液中有蓝色沉淀生成
B. 有气体生成
C. 有红色物质析出
D. 钠熔成小球浮游在液面上
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com