
食品抗氧化剂是能阻止或延缓食品氧化变质、提高食品稳定性和延长贮存期的食品添加剂。BHT是一种常用的食品抗氧化剂,合成方法有如下两种:

下列说法不正确的是

C.BHT不能与NaHCO3溶液反应生成CO2
D.两种方法的反应类型都是加成反应
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案科目:高中化学 来源: 题型:
甲、乙为单质,丙、丁为化合物,它们之间存在如图所示的转化关系。
(1)若甲、乙均为非金属,丙为氧化物,则:
 ①乙为氧化产物时,乙可能是________(填化学式,下同),按照元素周期表推测,此时反应物甲可能是__________________________________。
①乙为氧化产物时,乙可能是________(填化学式,下同),按照元素周期表推测,此时反应物甲可能是__________________________________。
②乙为还原产物时,丁所属的物质类别是___________________________________。
(2)若该转化关系为我国古代湿法冶炼金属乙的原理,写出此反应的化学方程式:__________________________________。若该转化关系为高温火法冶炼金属乙的原理,且同时生成的丁是一种有刺激性气味的气体,则丙可能为________________________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列有关醋酸的叙述中不正确的是( )
A.pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-)
B.浓度均为0.1 mol·L-1的CH3COOH溶液和CH3COONa溶液等体积混合后:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]
C.将pH=a的醋酸稀释为pH=a+1的过程中, 不断减小
不断减小
D.等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,a+b=14
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp(25 ℃)
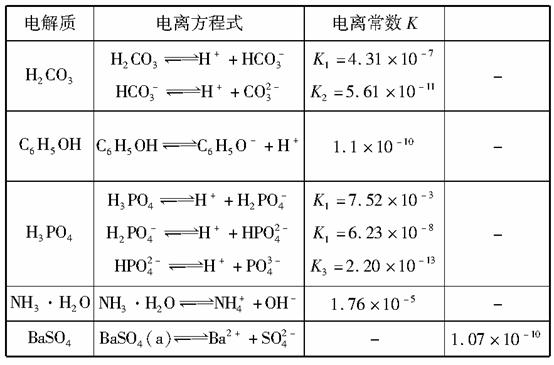
回答下列问题:
(1)写出C6H5OH与Na3PO4反应的离子方程式:__________。
(2)25 ℃时,向10 mL 0.01 mol·L-1 C6H5OH溶液中滴加V mL 0.01 mol·L-1氨水,混合溶液中粒子浓度关系正确的是________(填序号)。
a.若混合液pH>7,则V≥10
b.V=5时,2c(NH3·H2O)+2c(NH )=c(C6H5O-)+c(C6H5OH)
)=c(C6H5O-)+c(C6H5OH)
c.V=10时,混合液中水的电离程度小于0.01 mol·L-1 C6H5OH溶液中水的电离程度
d.若混合液pH<7,则c(NH )>c(C6H5O-)>c(H+)>c(OH-)
)>c(C6H5O-)>c(H+)>c(OH-)
(3)水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义。25 ℃时,Na2CO3第一步水解反应的水解常数Kh=________mol·L-1。
(4)如图所示,有T1、T2不同温度下两条BaSO4在水中的沉淀溶解平衡曲线(已知BaSO4的Ksp随温度升高而增大)。

①T2________25℃(填“>”、“<”或“=”)。
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是________(填序号)。
a.加入Na2SO4不能使溶液a点变为b点
b.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
c.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
d.升温可使溶液由b点变为d点
查看答案和解析>>
科目:高中化学 来源: 题型:
硫代硫酸钠在工业生产中用途非常广泛。
(1) 溶液是定量实验中的常用试剂。实验室需用480mL一定浓度的
溶液是定量实验中的常用试剂。实验室需用480mL一定浓度的 溶液,配制该溶液所需玻璃仪器除烧杯、量筒、玻璃棒外,还需__________________。
溶液,配制该溶液所需玻璃仪器除烧杯、量筒、玻璃棒外,还需__________________。
(2) 可以用作氰化物的解毒剂,工业上常用硫化碱法制备
可以用作氰化物的解毒剂,工业上常用硫化碱法制备 ,反应原理为:
,反应原理为:

某研究小组在实验室模拟该工业原理制备 ,部分实验装置如下:
,部分实验装置如下:

①装置B的作用是检验装置A中 的吸收效率,则B中试剂是________________,
的吸收效率,则B中试剂是________________,
表明 吸收效率低的实验现象是B中溶液________________________。
吸收效率低的实验现象是B中溶液________________________。
②实验结束时,测得装置C中的溶液含有两种溶质,其中一种为NaOH,则实验过程中该装置内发生反应的化学方程式是_________________________;若两种溶质的物质的量相等,则该溶液所含离子浓度的大小顺序为__________________________________。
③假设本实验所用的 含少量NaC1、NaOH,设计实验方案进行检验。请完成下表。
含少量NaC1、NaOH,设计实验方案进行检验。请完成下表。
已知:室温时CaCO3饱和溶液的pH=10.2。
限选试剂及仪器:稀硝酸、AgNO3溶液、CaC12溶液、酚酞溶液、蒸馏水、pH计,烧杯、试管、胶头滴管。

查看答案和解析>>
科目:高中化学 来源: 题型:
若NA表示阿伏加德罗常数,下列叙述中不正确的是
A.16 g O2与O3混合物中所含电子数为8NA
B.标准状况下,2.24 L CH3OH分子中共用电子对数为0.5NA
C.6 g SiO2晶体中硅氧共价键数为0.4NA
D.0.1 mol 13C18O中所含中子数为1.7NA
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,将CO和O2的混合气体26g充入一体积固定不变的密闭容器(容器内有足量的Na2O2固体),此时容器的压强为p1,用电火花不间断的点燃,使其充分反应,恢复至原温,结果固体增重14g,此时容器的压强为p2,则p1/p2为
A.9:4 B.7:3 C.7:6 D.6:7
查看答案和解析>>
科目:高中化学 来源: 题型:
有报道称,2013年太阳能晶体硅供不应求情况恐持续,其价格可望持稳。下列有关硅及其化合物的说法中正确的是 ( )
A.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞试剂瓶中
B.反应①Na2SiO3+H2O+CO2===Na2CO3+H2SiO3↓,反应②Na2CO3+SiO2 Na2SiO3+CO2↑,两反应是相互矛盾的,不可能都能发生
Na2SiO3+CO2↑,两反应是相互矛盾的,不可能都能发生
C.普通玻璃、石英玻璃,水泥等均属于硅酸盐材料
D.祖母绿的主要成分为Be3Al2Si6O18,用氧化物形式表示为3BeO·Al2O3·6SiO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com