
| A. | 将铜屑加入Fe3+溶液中:2Fe3++Cu═2Fe2++Cu2+ | |
| B. | 碳酸钠水解:CO32-+H2O═HCO3-+OH- | |
| C. | 食醋滴到鸡蛋壳上:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 将铜粉加入稀硫酸中:Cu+2H+═Cu2++H2↑ |
分析 A、离子方程式要满足电荷守恒和质量守恒;
B、盐的单水解要用可逆号;
C、醋酸是弱酸;
D、铜和稀硫酸不反应.
解答 解:A、离子方程式要满足电荷守恒和质量守恒,此离子方程式均满足,且符合反应实际,故A正确;
B、盐的单水解程度很小,不彻底,故要用可逆号,应为CO32-+H2O?HCO3-+OH-,故B错误;
C、醋酸是弱酸,不能拆,故离子方程式应为:CaCO3+2CH3COOH═Ca2++CO2↑+H2O+2CH3COO-,故C错误;
D、铜在金属活动性顺序表中处于H元素之后,故铜和稀硫酸不反应,不能将氢气置换出,即此离子方程式不符合实际,故D错误.
故选A.
点评 本题考查离子方程式书写原则的分析,正误判断方法,注意电荷守恒,原子守恒的应用,题目难度中等.注意D选项反应是否符合实际.


科目:高中化学 来源: 题型:选择题
| A. | 将碘酒滴到土豆片上,土豆片变蓝,说明碘元素均遇淀粉变蓝 | |
| B. | 工业上常用油脂在碱性条件下的水解反应来制肥皂 | |
| C. | 加热条件下,葡萄糖溶液能与新制Cu(OH)2悬浊液反应产生砖红色沉淀 | |
| D. | 蛋白质在浓硝酸作用下能发生颜色反应,可用来鉴别部分蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正常雨水PH等于7,酸雨的PH小于7 | |
| B. | 金属钠着火燃烧时,可用泡沫灭火器灭火 | |
| C. | 在放电条件下,氮气和氧气化合生成二氧化氮 | |
| D. | 冷的浓硫酸与铁、铝反应时会使金属表面生成致密的氧化物而钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g D2O和18 g H2O中含有的质子数均为10NA | |
| B. | 1 mol Cu和2mol热的浓硫酸反应可生成NA个SO2分子 | |
| C. | 3 mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| D. | 标准状况下,22.4 L N2和H2混合气中含NA个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
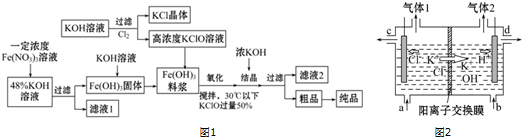
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打Na2CO3,苛性钠NaOH | B. | 明矾KAl(SO4)2•12H2O,消石灰Ca(OH)2 | ||
| C. | 苏打NaHCO3,石灰石CaCO3 | D. | 纯碱NaOH,食盐NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com