
| A. | W与X形成的化合物溶于水后溶液呈碱性 | |
| B. | 简单离子半径:W<X<Z | |
| C. | 气态氢化物的热稳定性:W<Y | |
| D. | 最高价氧化物的水化物的酸性:Y>Z |
分析 四种短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是短周期主族元素原子中最大的,则X为Na.由原子序数可知,Y、Z处于第三周期,而Z与X(钠)形成的离子化合物的水溶液呈中性,则Z为Cl.W、X的简单离子具有相同电子层结构,且W与Y同族,W在第二周期且是非金属元素,W可能是氮(或)氧,则对应的Y为磷(或硫).
解答 解:四种短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是短周期主族元素原子中最大的,则X为Na.由原子序数可知,Y、Z处于第三周期,而Z与X(钠)形成的离子化合物的水溶液呈中性,则Z为Cl.W、X的简单离子具有相同电子层结构,且W与Y同族,W在第二周期且是非金属元素,W可能是氮(或)氧,则对应的Y为磷(或硫).
A.W可能是氮或氧,与钠形成的化合物可能是氮化钠,氧化钠,过氧化钠,它们与水反应都能生成氢氧化钠使溶液呈碱性,故A正确;
B.X离子(Na+)、W离子的电子层为2层,Z离子(Cl-)电子层为3层,电子层结构相同,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故简单离子半径大小顺序是:X<W<Z,故B错误;
C.W与Y处于同于主族,从上到下非金属性逐渐减弱,气态氢化物的热稳定性:W>Y,故C错误;
D.Y与Z处于同同期,从左到右非金属性逐渐增强,最高价氧化物的水化物的酸性:Z>Y,故D错误.
故选:A.
点评 本题考查结构性质位置关系应用,侧重对元素周期律的考查,正确推断各元素为解答关键,注意元素的不确定性,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 6.72L | B. | 5.6L | C. | 2.8L | D. | 13.44L |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾和漂白粉均可用于自来水的杀菌、消毒 | |
| B. | 用丁达尔实验可以将Al(OH)3胶体和NaCl溶液区分 | |
| C. | CCl4萃取碘水中的I2,先从分液漏斗下口放出有机层,后从分液漏斗下口放出水层 | |
| D. | 浓盐酸与MnO2反应制备纯净Cl2,气体产物先通过浓硫酸,后通过饱和食盐水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| B. | 氯化钠是电解质,可电解其水溶液获得金属钠 | |
| C. | SO2有还原性,常用来漂白纸浆 | |
| D. | 四氯化碳密度比水大,可用于萃取溴水中的溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
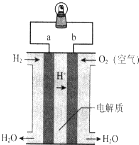
| A. | a电极是正极 | B. | 电流由b通过灯泡流向a | ||
| C. | 该电池总反应是2H2+O2═2H2O | D. | 该装置可将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16 | B. | 32 | C. | 48 | D. | 64 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com