
常温下,往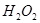 溶液中滴加少量
溶液中滴加少量 溶液,可发生如下两个反应:
溶液,可发生如下两个反应: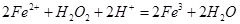 ,
,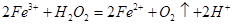 下列说法正确的是
下列说法正确的是
A.在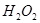 分解过程中,
分解过程中,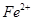 和
和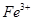 的总量保持不变
的总量保持不变
B.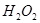 的氧化性比
的氧化性比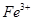 强,其还原性比
强,其还原性比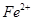 弱
弱
C.在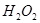 分解过程中,溶液的
分解过程中,溶液的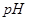 逐渐下降
逐渐下降
D.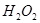 生产过程中加入少量
生产过程中加入少量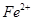 可以提高产率
可以提高产率
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:


 NH3?H2O
NH3?H2O NH4++OH-
NH4++OH- NH3?H2O
NH3?H2O NH4++OH-
NH4++OH-查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2O2在上述两个反应在都只做氧化剂 | B、在H2O2分解过程中,溶液C(H+)不变 | C、在H2O2分解过程中,Fe2+和Fe3+的总量保持不变 | D、H2O2生产过程要严格避免混入Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2O2氧化性比Fe3+强,其还原性比Fe2+强 | B、在反应前和反应完成后,溶液pH保持不变 | C、H2O2的生成过程要严格避免混入Fe3+或Fe2+ | D、反应中,Fe3+和Fe2+总物质的量始终在改变 |
查看答案和解析>>
科目:高中化学 来源:四川省绵阳中学2011届高三化学考前热点训练:06化学常用计量与氧化还原反应 题型:013
|
常温下,往过氧化氢中滴加少量FeSO4溶液,可发生如下两个反应: ①2Fe2++H2O2+2H+ ②2Fe3++H2O2 下列关于反应历程的说法不合理的是 | |
| [ ] | |
A. |
H2O2氧化性比Fe3+强,其还原性比Fe2+强 |
B. |
在反应前和反应完全后,溶液pH保持不变 |
C. |
H2O2的生产过程要严格避免混入Fe2+ |
D. |
反应过程中,Fe2+和Fe3+,总物质的量始终在改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com