
【题目】下列离子中所有原子都在同一平面上的一组是( )
A.![]() 和
和![]() B.
B.![]() 和
和![]()
C.![]() 和
和![]() D.
D.![]() 和
和![]()
【答案】C
【解析】
A. ![]() 中心原子的价电子对数=2+
中心原子的价电子对数=2+![]() =3,含有一个孤对电子对,空间构型为V型,
=3,含有一个孤对电子对,空间构型为V型,![]() 中心原子的价电子对数=4+
中心原子的价电子对数=4+![]() =4,没有孤对电子对,空间构型为正四面体,选项A错误;
=4,没有孤对电子对,空间构型为正四面体,选项A错误;
B. ![]() 中心原子的价电子对数=3+
中心原子的价电子对数=3+![]() =4,含有一个孤对电子对,空间构型为三角锥形,
=4,含有一个孤对电子对,空间构型为三角锥形,![]() 中心原子的价电子对数=3+
中心原子的价电子对数=3+![]() =4,含有一个孤对电子对,空间构型为三角锥形,选项B错误;
=4,含有一个孤对电子对,空间构型为三角锥形,选项B错误;
C. ![]() 中心原子的价电子对数=3+
中心原子的价电子对数=3+![]() =3,没有孤对电子对,空间构型为平面三角形,
=3,没有孤对电子对,空间构型为平面三角形,![]() 中心原子的价电子对数=3+
中心原子的价电子对数=3+![]() =3,没有孤对电子对,空间构型为平面三角形,选项C正确;
=3,没有孤对电子对,空间构型为平面三角形,选项C正确;
D. ![]() 中心原子的价电子对数=4+
中心原子的价电子对数=4+![]() =4,没有孤对电子对,空间构型为正四面体,
=4,没有孤对电子对,空间构型为正四面体,![]() 中心原子的价电子对数=4+
中心原子的价电子对数=4+![]() =4,没有孤对电子对,空间构型为正四面体,选项D错误。
=4,没有孤对电子对,空间构型为正四面体,选项D错误。
答案选C。


科目:高中化学 来源: 题型:
【题目】t℃时,向20.00mL0.1mol/L二元弱酸H2X溶液中滴入0.1mol/LNaOH溶液,溶液中由水电离出的c水(OH-)的负对数[-lgc 水(OH-)]与所加NaOH溶液体积的关系如图所示。下列说法中不正确的是
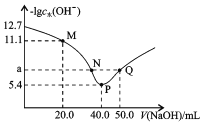
A.M点溶液中:c(Na+)>c(HX-)>c(H2X)
B.P点溶液中: c(OH-)-c(H+)=c(HX-)+2c(H2X)
C.溶液中![]()
D.水的电离程度:P>N=Q>M,且a=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.下表是从实验中测得的不同物质中氧氧键的键长和键能数据:
氧氧键 |
|
|
|
|
键长 | 149 | 128 | 121 | 112 |
键能 |
|
|
|
|
其中![]() 、
、![]() 的值尚未测定,但可根据规律推导
的值尚未测定,但可根据规律推导![]() 、
、![]() 、
、![]() 、
、![]() 的大小顺序是
的大小顺序是![]() ,该规律是( )
,该规律是( )
A.成键时,电子数越多,键能越大
B.键长越短,键能越大
C.成键所用电子数越少,键能越大
D.成键时电子对越偏移,键能越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是金属钨晶体中的一个晶胞的结构模型(原子间实际是相互接触的)。它是一种体心立方结构。实验测得金属钨的密度为19.30g·cm-3,钨的相对原子质量为183.9.假定金属钨为等直径的刚性球,请回答以下各题:
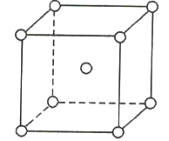
(1)每一个晶胞中分摊到__________个钨原子。
(2)计算晶胞的边长a。_____________
(3)计算钨的原子半径r(提示:只有体对角线上的各个球才是彼此接触的)。___________
(4)计算金属钨原子采取的体心立方密堆积的空间利用率。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下反应:Fe3++AgFe2++Ag+的平衡常数K=0.3。现将含0.010mol/LFe(NO3)2和0.10mol/L Fe(NO3)3的混合溶液倒入烧杯甲中,将含0.10mol/L的AgNO3溶液倒入烧杯乙中(如图),闭合开关 K,关于该原电池的说法正确的是
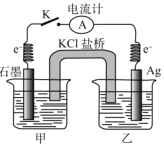
A.原电池发生的总反应中Ag+氧化Fe2+
B.盐桥中阳离子从左往右作定向移动
C.石墨为负极,电极反应为Fe2+-e-= Fe3+
D.当电流计指针归零时,总反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为NaCl和CsCl的晶体结构,下列说法错误的是( )
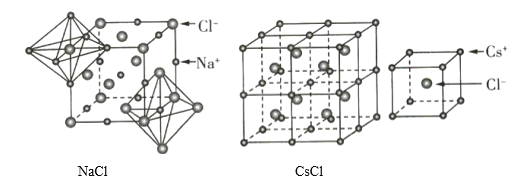
A.NaCl和CsCl都属于AB型的离子晶体
B.NaCl和CsC1晶体中阴、阳离子个数比相同,所以二者的阴、阳离子的配位数也相同
C.CsCl晶体中阴、阳离子的配位数均为8
D.NaCl和CsCl都属于AB型的离子晶体,但阴、阳离子的半径比不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法不正确的是( )

A. 该晶体属于离子晶体
B. 晶体的化学式为Ba2O2
C. 该晶体晶胞结构与NaCl相似
D. 与每个Ba2+距离相等且最近的Ba2+共有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知高锰酸钾与重铬酸钾(K2Cr2O7)都是化学中常用的强氧化剂,高锰酸钾溶液呈紫红色而重铬酸钾溶液中存在如下平衡:2CrO42-(黄色)+2H+![]() Cr2O72-(橙色)+H2O,若要使溶液的橙色加深,下列可采用的方法是( )
Cr2O72-(橙色)+H2O,若要使溶液的橙色加深,下列可采用的方法是( )
A.加入适量小苏打B.加入适量稀硝酸
C.加入适量烧碱固体D.加水稀释
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是
A.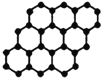 24g石墨烯中含有C-C键的个数为3NA
24g石墨烯中含有C-C键的个数为3NA
B.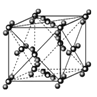 88g干冰中含有NA个晶胞结构单元
88g干冰中含有NA个晶胞结构单元
C.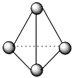 62gP4含有P-P键的个数为6NA
62gP4含有P-P键的个数为6NA
D.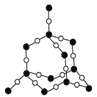 60gSiO2中含有Si-O键的个数为2NA
60gSiO2中含有Si-O键的个数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com