
将下列各组物质按单质、氧化物、酸、碱、盐分类顺序排列,其中正确的是 ( )
A.银、干冰、硫酸、烧碱、食盐
B.碘酒、冰、盐酸、烧碱、食盐
C.氢气、二氧化硫、硝酸、纯碱、硝酸钾
D.铜、氧化铜、醋酸、石灰水、氯化铜
科目:高中化学 来源: 题型:
利用一种新型陶瓷(能传递H+),实现了氨的电化学合成。该过程N2和H2的转化率远高于现在工业上使用的氨合成法。对于电化学合成氨的有关叙述正确的是( )
A.N2在阴极上被氧化 B.可选用铁作为阳极材料
C.阳极的电极反应式是N2+6H++6e-===2NH3
D.该过程的总反应式是N2+3H2  2NH3
2NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
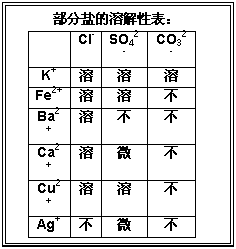
某混合物澄清透明的水溶液中,可能含有以下
离子中若干种:K+、Ca2+、Fe2+、Cu2+、Cl-、CO32-、
SO42-,现每次取该溶液100.00ml溶液进行以下实验:
①第一份加入AgNO3溶液发现有沉淀生成;
②第二份加足量BaCl2溶液生成沉淀,洗涤后干燥
得沉淀6.27g,再将该沉淀加入足量盐酸溶解后再过滤洗
涤干燥得沉淀2.33g.
请回答下列问题:
(1)根据以上实验判断,原溶液中一定不存在的
离子是 ,可能存在的离子是 。
(2)原溶液中一定存在的阳离子是 ,其物质的量浓度至少为 mol/l.
(3)原溶液中一定存在的阴离子是 ,其物质的量浓度分别为 mol/l、
mol/l.。
查看答案和解析>>
科目:高中化学 来源: 题型:
往含0.2 mol KOH和0.1 mol Ca(OH)2的溶液中持续地通入CO2气体,当通入气体的体积为6.72 L(标准状况)时立即停止,则在这一过程中,溶液中离子的物质的量n和通入CO2的体积V的关系示意图正确的是(气体的溶解忽略不计) ( )
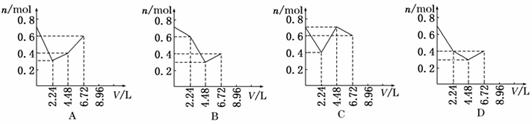
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色溶液,其中可能存在的离子有:Na+、Ag+、Ba2+、Fe3+、Al3+、AlO2-、
S2-、SO32-、CO32-、SO42-,现取该溶液进行实验,实验结果如下:
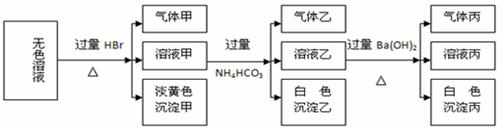
试回答下列问题:
(1)生成沉淀甲的离子方程式为: 。
(2)由溶液甲生成沉淀乙的离子方程式为 。
(3)已知气体甲由两种氧化物组成(不包括水蒸汽和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入下表(表中每一行对应正确即可得分)
| 步骤 | 实验目的 | 试剂 | 现象 |
| 1 | |||
| 2 | |||
| 3 | 检验CO2 | 澄清石灰水 | 溶液变浑浊 |
(4)综上所述,该溶液肯定存在的离子有: 。
(5)针对溶液中可能存在的离子,用实验证明是否存在的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
两个体积相同的容器,一个盛有二氧化氮(NO2),另一个盛有氮气和氧
气,在同温同压下两容器内的气体一定具有相同的 ( )
A.原子总数 B.质子总数 C.分子总数 D.质量
查看答案和解析>>
科目:高中化学 来源: 题型:
混合气体由N2和CH4组成,测得混合气体在标准状况下的密度为0.821g/L,则混合气体中N2和CH4的体积之比为( )
A.5:1 B.1:4 C.4:1 D.1:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学——选修3:物质结构】(15分)
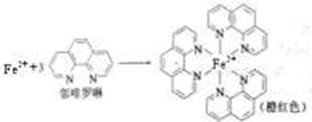 |
 4FeCl2+N2O↑+6HCl+H2O
4FeCl2+N2O↑+6HCl+H2O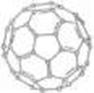
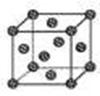
图1 图2
(4)① 有机太阳能固体电池材料含有高纯度C60,其结构如图1,则1 mol C60分子中π键的数目为 ,C60的晶胞结构如图2,则其配位数为_______若此晶胞的密度为ρg/cm3则两个最近C60间的距离为________cm(列式表达,已知阿伏伽德罗常数为NA)
② 如果把晶胞顶点与最近三个面心所围成的空隙叫做四面体空隙,第四周期电负性最小的原子可作为容体掺入C60晶体的空隙中,形成具有良好的超导性的掺杂C60化合物。若每个四面体空隙填入一个原子,则全部填满C60晶体的四面体空隙后,所形成的掺杂C60化合物的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
请完成下面两个小题:
Ⅰ.(6分)反应m A+n B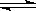 p C在某温度下达到平衡。
p C在某温度下达到平衡。
① 若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系是______ _________。
② 若C为气体,且m + n = p,在加压时化学平衡发生移动,则平衡必定向_____方向移动。
③ 如果在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为_____态。.
Ⅱ.(11分)在一定温度下,在一体积固定的密闭容器中加入2 mol X和1 mol Y,发生如下反应:
2X(g)+Y(g)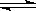 a Z(g)+W(g) ΔH=-Q kJ·mol-1(Q>0)
a Z(g)+W(g) ΔH=-Q kJ·mol-1(Q>0)
当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;平衡后再升高温度,混合气体的平均相对分子质量减小,则
(1)温度升高,平衡常数K的值是____________(填“增大”、“减小”或“不变”)。
(2)化学计量数a的值为____________(a为整数)。
(3)有同学认为,Q1一定小于Q,你认为该结论是否正确?____(填“是或否”)其理由是__________________________________。
(4)维持温度不变,能引起c(X)/c(W)减小的操作有( )
A.加入X
B.加入Y
C.增大压强
D.充入He气
(5)X的转化率α=____________(用含Q、Q1的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com