
【题目】A是一种重要的化工原料,部分性质及转化关系如下图:

请回答:
(1)D中官能团的名称是_____________。
(2)A→B的反应类型是________________。
A.取代反应B.加成反应 C.氧化反应 D.还原反应
(3)写出A→C反应的化学方程式_______________________。
(4)某烃X与B是同系物,分子中碳与氢的质量比为36:7,化学性质与甲烷相似。现取两支试管,分别加入适量溴水,实验操作及现象如下:
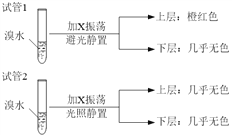
有关X的说法正确的是_______________________。
A.相同条件下,X的密度比水小
B.X的同分异构体共有6种
C.X能与Br2发生加成反应使溴水褪色
D.试验后试管2中的有机层是上层还是下层,可通过加水确定
【答案】 羧基 BD CH2=CH2+H2O![]() CH3CH2OH AD
CH3CH2OH AD
【解析】C与D反应生成乙酸乙酯,则C、D分别为乙酸、乙醇中的一种,A与水反应生成C,A氧化生成D,且A与氢气发生加成反应生成B,可推知A为CH2=CH2,与水在一定条件下发生加成反应生成C为CH3CH2OH,乙烯氧化生成D为CH3COOH,乙烯与氢气发生加成反应生成B为CH3CH3。
(1)D为CH3COOH,含有的官能团为羧基,故答案为:羧基;
(2)A→B是乙烯与氢气发生加成反应生成乙醇,也属于还原反应,故选:BD;
(3)A→C反应的化学方程式:CH2=CH2+H2O![]() CH3CH2OH,故答案为:CH2=CH2+H2O
CH3CH2OH,故答案为:CH2=CH2+H2O![]() CH3CH2OH;
CH3CH2OH;
(4)某烃X与B(乙烷)是同系物,分子中碳与氢的质量比为36:7,则C、H原子数目之比为![]() :
:![]() =3:7=6:14,故X为C6H14。A.相同条件下,C6H14的密度比水小,故A正确;B.C6H14的同分异构体有己烷、2-甲基戊烷、3-甲基戊烷、2,3-二甲基丁烷、2,2-二甲基丁烷,共5种,故B错误;C.X为烷烃,不能与溴发生加成反应,故C错误;D.发生取代反应得到溴代烃,与水不互溶,可以可通过加水确定试管2中的有机层是上层还是下层,故D正确;故选AD。
=3:7=6:14,故X为C6H14。A.相同条件下,C6H14的密度比水小,故A正确;B.C6H14的同分异构体有己烷、2-甲基戊烷、3-甲基戊烷、2,3-二甲基丁烷、2,2-二甲基丁烷,共5种,故B错误;C.X为烷烃,不能与溴发生加成反应,故C错误;D.发生取代反应得到溴代烃,与水不互溶,可以可通过加水确定试管2中的有机层是上层还是下层,故D正确;故选AD。


科目:高中化学 来源: 题型:
【题目】有关电解质的说法正确的是( )
A.纯水的导电性很差,所以水不是电解质
B.SO3水溶液的导电性很好,所以SO3是电解质
C.液态的铜导电性很好,所以铜是电解质
D.Na2O液态时能导电,所以Na2O是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性硼化钒—空气电池工作时反应为:4VB2+11O2===4B2O3+2V2O5,室温下用该电池为电源,用惰性电极电解饱和氯化钠溶液,装置如图。当外电路中通过0.04 mol电子时,乙装置中溶液的体积为400 mL。则下列说法正确的是
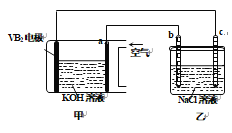
A. 外电路中电子由a电极流向b电极
B. c电极上生成气体的体积为4.48 L
C. 乙装置中溶液的pH为13
D. VB2电极发生的电极反应为:2VB2+11H2O―22e-===V2O5+2B2O3+22H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铜纳米颗粒和银纳米颗粒相隔一定距离固定在石墨片上,然后浸在AgNO3溶液中,可构成一种纳米型原电池。该电池负极发生的反应为( )
A. Ag++e—===Ag
B. Cu-2e—===Cu2+
C. Cu2++2e—===Cu
D. 2H++2e—===H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液体燃料电池相对于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,H2SO4作为电解质。下列关于该燃料电池的叙述正确的是 ( )
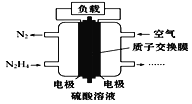
A. 电流从左侧电极经过负载后流向右侧电极
B. 该燃料电池正极发生的电极反应式为N2H4-4e-N2↑+4H+
C. 利用该燃料电池工业上可以电解熔融MgCl2 制备Mg
D. 该燃料电池持续放电时,右侧电池区中因电极反应消耗H+,故c(H+)逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某锂离子电池工作原理如下图所示,电池反应为:Li1-xCoO2+LixC![]() LiCoO2+C。下列说法不正确的是
LiCoO2+C。下列说法不正确的是
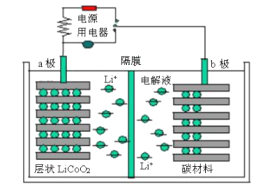
A. 放电时,电子从b极经用电器流向a极
B. 放电时,若转移1mol e-,碳材料将增重7 g
C. 充电时,锂离子通过隔膜进入右室
D. 充电时,a极反应:LiCoO2-xe-= Li1-xCoO2+xLi+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒是一种熔点高、硬度大、无磁性的金属,广泛应用于钢铁、航空航天、能源、化工等领域。目前工业上使用一种新工艺,以便从冶炼铝的固体废料一赤泥中提取金属钒,赤泥主要含有Fe2O3、Al2O3、V2O5和CuO,具体工艺流程图如下:
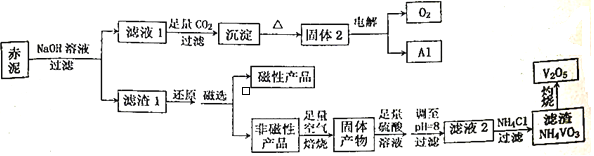
已知:钒有多种价态,其中+5价最稳定。钒在溶液中主要以VO2+和VO3-的形式存在,且存在平衡VO2++H2O![]() VO3-+2H+。回答下列问题:
VO3-+2H+。回答下列问题:
(1)磁性产品的化学式为_________________________。
(2)赤泥加入NaOH溶液,发生的离子反应方程式为___________________。能否用氨水代替NaOH溶液,___________(填“能”或“不能”),理由是___________________________________________。
(3)滤液1生成沉淀的离子反应方程式为_________________________________________。
(4)调至pH=8的目的有两个,一是___________________,二是使VO2+转化为VO3-,此时溶液中VO2+和VO3-的物质的量之比为a:b,VO2++H2O![]() VO3-+2H+的平衡常数K=____________________。
VO3-+2H+的平衡常数K=____________________。
(5)滤液2加氯化铵生成NH4VO3的离子方程式为__________________________,该反应能发生是因为__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com