
A.40 W g B.![]() g C.5(m-n) g D.m g
g C.5(m-n) g D.m g
科目:高中化学 来源: 题型:
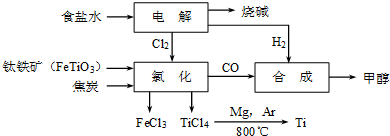
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用H2 还原mgCuO,当大部分固体变红时停止加热,冷却后称量,知残留固体质量为 ng,共用去WgH2 ,则被还原的CuO的质量为
A.40Wg B.g C.5(m-n)g D.mg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com