
| A. | NaCl | B. | H2S | C. | Na2S | D. | NH4Cl |
分析 水的电离方程式为H2O?H++OH-,加入的物质或离子能影响水电离平衡的移动,则破坏水的电离.
解答 解:A、氯化钠电离出的钠离子和氯离子均不能与水电离出的氢离子和氢氧根离子结合,不影响水的电离,故A选;
B、硫化氢电离出的氢离子,抑制水的电离,破坏水的电离平衡,故B不选;
C、硫化钠电离出的硫离子结合水电离出的氢离子,破坏水的电离平衡,故C不选;
D、氯化铵电离出的铵根结合水电离出的氢氧根离子,破坏水的电离平衡,故D不选,
故选A.
点评 本题考查了水的电离,酸或碱能抑制水的电离,含有弱根离子的盐能促进水的电离,根据溶液中氢离子和氢氧根离子浓度是否变化来确定是否破坏水的电离,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7 | |
| B. | 将等体积pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水量多 | |
| C. | 常温下,向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+)=c(Cl-) | |
| D. | 0.2 mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
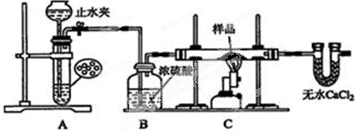
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 这三种物质都属于气态烃 | |
| B. | 乙炔中碳的质量分数最小 | |
| C. | 溴水能与乙烯和乙炔加成,但不能与乙烷反应 | |
| D. | 一个分子中,共用电子对最多的物质是乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1-丙醇与浓氢溴酸反应:CH3CH2 CH2OH+HBr$\stackrel{△}{→}$CH3CH2 CH2Br+H2O | |
| B. | 1-溴丙烷与氢氧化钠溶液共热:CH3CH2 CH2Br+NaOH$→_{△}^{水}$CH3CH2 CH2OH+NaBr | |
| C. | 苯酚钠中通入少量二氧化碳:2 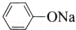 +CO2+H2O→2 +CO2+H2O→2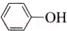 +Na2CO3 +Na2CO3 | |
| D. | 蔗糖在稀硫酸作用下水解:C12H22O11(蔗糖)+H2O$→_{△}^{稀硫酸}$C6H12O6(果糖)+C6H12O6(葡萄糖) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液中滴入AgNO3溶液,产生白色沉淀,该溶液中一定含Cl- | |
| B. | 某溶液与淀粉碘化钾溶液反应后显蓝色,证明溶液是氯水或溴水 | |
| C. | 将氟气通入氯化钠水溶液中,一定有氢氟酸和O2生成 | |
| D. | 实验证明氯水也能导电,所以氯水是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定浓度的醋酸钠溶液可使酚酞溶液变红,其原因是发生了如下反应:CH3COO-+H2O?CH3COOH+OH-,使得溶液中的c(OH-)>c(H+) | |
| B. | 在常温下,10 mL 0.2 molL-1盐酸与10 mL 0.2 molL-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=13 | |
| C. | 在0.1 molL-1 NH4Cl溶液中:c(H+)+c(NH4+)=c(Cl-) | |
| D. | 5 mL 1 molL-1 CH3COONa溶液与5 mL 1 molL-1盐酸混合液中c(Cl-)=c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com