
卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。以卤块为原料可制得轻质氧化镁,工艺流程如下图:
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。若要求产品尽量不含杂质,请根据表1表2提供的资料,填写空白:
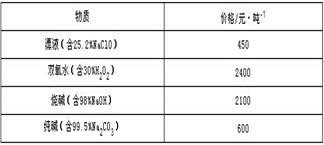
表1 生成氢氧化物沉淀的pH 表2 化学试剂价格表
| 试剂 | 价格(元/吨) |
| 漂液(含NaClO,25.2%) | 450 |
| 双氧水(含H2O2 ,30%) | 2400 |
| 烧碱(含98% NaOH) | 2100 |
| 纯碱(含99.5% Na2CO3) | 600 |
|
(1)在步骤②中加入的试剂X,最佳的选择是 ,原因是 。写出加入X发生反应的离子方程式 。选择 (试剂)来检验Fe2+是否完全氧化为Fe3+
(2)在步骤③中控制pH=9.8,其目的是 。
(3)试剂Z应该是 。
(4)在步骤⑤中发生反应的化学方程式是 。
(5)若在实验室中完成步骤⑥,则沉淀物必需在仪器A中灼烧。A应放置于仪器B上灼烧,灼烧完毕后应用仪器C取下仪器A置于仪器D上冷却。则B、C、D分别是 、 、
。
【答案解析】(14分)(1)漂液,漂液比H2O2的价格低得多。 (2分)
2Fe2+ + ClO-+ 2H+ = 2Fe3+ + Cl-+ H2O (2分)K3[Fe(CN)6]溶液(2分)
(2)使除Mg2+以外的各种杂质金属离子都生成氢氧化物沉淀,以便过滤除去。(2分)
(3)纯碱 (2分)
(4)MgCO3 +H 2O 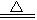 Mg(OH)2↓+ CO2↑ (2分,产物写成碱式碳酸镁也算正确)
Mg(OH)2↓+ CO2↑ (2分,产物写成碱式碳酸镁也算正确)
(5)泥三角、坩埚钳、石棉网 (2分,对两个得1分)
解析:(1)Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去;X是氧化剂,漂液和双氧水都是氧化剂,从经济角度考虑,选择价格低的漂液;次氯酸跟将亚铁离子氧化成铁离子,本身被还原成氯离子,根据得失电子守恒配平,离子方程式为:2Fe2+ + ClO-+ 2H+ = 2Fe3+ + Cl-+ H2O;再用K3[Fe(CN)6]溶液来检验Fe2+是否完全被氧化;(2)参照表格,在步骤③中控制pH=9.8,其目的是使除Mg2+以外的各种杂质金属离子都生成氢氧化物沉淀,以便过滤除去;
(3)试剂Z的作用是将镁离子转化成沉淀,烧碱和纯碱都可以,从经济角度分析还是要选择纯碱;
(4)沉淀物B是碳酸镁,要将它转化为氢氧化镁再分解成氧化镁,所以在步骤⑤中发生反应的化学方程式是:MgCO3 +H 2O  Mg(OH)2↓+ CO2↑
Mg(OH)2↓+ CO2↑
(5)灼烧应在坩埚中进行,置于泥三角上,用坩埚钳取用,最后置于石棉网上冷却。
【思路点拨】本题属于简单工艺流程题,考查了基本实验操作、无机化合物性质、除杂,题目不难,平时注意基本实验操作的知识点,培养提取题目信息进行分析问题的能力。


 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
下列物质在水溶液中的电离方程式不正确的是
A.NaHSO4 ===Na++H++SO42-
B. AgCl ===Ag++ Cl-
C.Ba (OH)2 ===Ba2+ + 2OH-
D. CH3COONH4 NH4++ CH3COO-
NH4++ CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
①CaCO3= CaO + CO2 ΔH= +177.7 kJ·mol-1
②C(s) + H2O(g) = CO(g) + H2(g) ΔH= 131.3 kJ·mol-1
③1/2 H2SO4(aq) + NaOH(aq) = 1/2Na2SO4(aq) + H2O(l) ΔH= —57.3kJ
④C(s) + O2(g) = CO2(g) ΔH= —393.5 kJ·mol-1
⑤CO(g) + 1/2O2(g) = CO2(g) ΔH= —283 kJ·mol-1
⑥HNO3(aq) + NaOH(aq) = NaNO3(aq) + H2O(l) ΔH= —57.3 kJ·mol-1
(1)上述热化学方程式中,不正确的有 ;
(2)上述反应中,表示燃烧热的热化学方程式有 ;表示中和热的热化学方程式有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
固体粉末X中可能含有FeO、Fe2O3、MnO2、K2SO3、KAlO2、MgCl2、K2CO3、NaNO2中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如图所示:
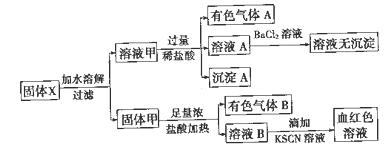
根据上述实验,以下说法正确的是
A.溶液甲中一定含有K2SO3、NaNO2
B.无法判断溶液中是否有K2SO3
C.气体A和气体B-定为混合物
D.原混合物中一定有Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
在C6H10O2的所有同分异构体中,能与Na2CO3溶液反应产生CO2气体的且能使溴的四氯化碳溶液褪色的有(不考虑顺反等立体异构)
A.8种 B.13种 C.17种 D.21种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A. 在标准状况下,1mol水的体积是22.4L
B. 1molH2所占的体积一定是22.4L
C. 在标准状况下,NA个任何分子所占的体积约为22.4L
D. 在标准状况下,总质量为28g N2和CO的混合气体,其体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度时,将1 mol A和2 mol B放入容积为5 L的某密闭容器中发生如下反应:A(s)+2B(g)  C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述不正确的是( )
C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述不正确的是( )
A.在5 min 内该反应用C的浓度变化表示的反应速率为0.02 mol/(L·min)
B.5 min 时,容器内D的浓度为0.2 mol/L
C.该可逆反应随反应的进行,容器内压强逐渐增大
D.5 min时容器内气体总的物质的量为3 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com