
| A.①② | B.②④⑤ | C.②④ | D.③⑤ |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
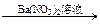 白色沉淀
白色沉淀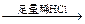 白色沉淀。
白色沉淀。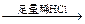 有无色气体生成
有无色气体生成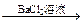 白色沉淀。
白色沉淀。 无色溶液
无色溶液 白色沉淀。
白色沉淀。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
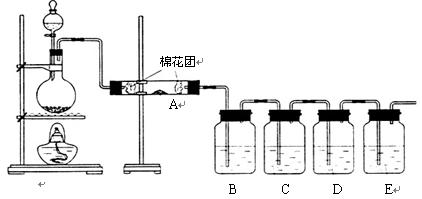
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
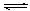 SO3(g);△H=" —98" kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K= 。
SO3(g);△H=" —98" kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K= 。 2SO3(g)达到平衡后改变下述条件SO3 的体积分数变大的是
2SO3(g)达到平衡后改变下述条件SO3 的体积分数变大的是 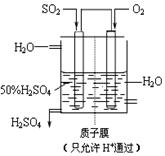
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.大于2x% | B.小于2x% | C.等于2x% | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②④ | B.③④ | C.③⑤ | D.①③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硫既可做氧化剂,又可做还原剂 | B.SO3只有氧化性,SO2只有还原性 |
| C.可以用铁罐贮运冷的浓硫酸 | D.氢硫酸既有氧化性,又有还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com