
| A. | 质子数为7、中子数为8的氮原子:${\;}_{7}^{8}$N | |
| B. | 氮原子的结构示意图: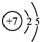 | |
| C. | 氨分子的电子式: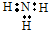 | |
| D. | 对硝基甲苯的结构简式:NO2CH3 |
分析 A.元素符号左上角为质量数,左下角为质子数,质量数=质子数+中子数;
B.氮原子是7号元素,核内质子数为7,核外有2个电子层,第一层2个电子,第二层5个电子,画出其原子的结构示意图即可;
C.氨气分子的电子式中漏掉了氮原子的1对未成键电子;
D.对硝基甲苯中苯环连接氮原子.
解答 解:A.质子数为7、中子数为8的氮原子:$\underset{\stackrel{15}{\;}}{7}N$,故A错误;
B.氮原子是7号元素,核内质子数为7,核外有2个电子层,第一层2个电子,第二层5个电子,氮原子的结构示意图为: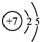 ,故B正确;
,故B正确;
C.氨气分子中氮原子最外层达到8电子稳定结构,漏掉了氮原子的一对孤电子对,氨气的电子式为 ,故C错误;
,故C错误;
D.对硝基甲苯的结构简式为: ,故D错误;
,故D错误;
故选B.
点评 本题考查了原子结构示意图、电子式、结构简式等知识,题目难度不大,注意掌握离子化合物与共价化合物的电子式区别,明确电子式、分子式、结构简式、结构式的正确表示方法,试题有利于培养学生灵活应用所学知识的能力.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
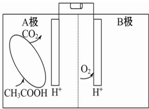
| A. | A极为正极,B极为负极 | |
| B. | 电池内电解质溶液中所含的H+由B极移向A极 | |
| C. | A极的电极反应为:CH3COOH-8e-+2H2O═2CO2↑+8H+ | |
| D. | 电池工作过程中,电解质溶液的pH会明显下降 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
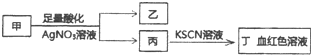
| A. | 若乙为白色沉淀,则甲可能含有SiO32- | |
| B. | 若乙为黄色沉淀,则甲可能为FeI3 | |
| C. | 若乙为浅黄色沉淀,则甲可能含有S2- | |
| D. | 若乙为浅黄色沉淀,则甲可能是FeBr2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用图1示装置制备Cl2 | |
| B. | 将混合气体通过装有NaOH溶液的洗气瓶除去Cl2中混有的HCl | |
| C. | 用图2示装置分离CH3COOC2H5与饱和Na2CO3溶液 | |
| D. | 称取1.06 g Na2CO3固体,置于100 mL容量瓶中,加水稀释,配制0.10 mol•L-1的Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

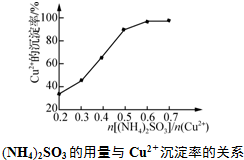 ,工业上$\frac{n[(N{H}_{4})_{2}S{O}_{3}]}{n(C{u}^{2+})}$采用0.6最为适宜,此时(NH4)2SO3略过量,其原因是保证生成的CuCl不被氧气氧化或(NH4)2SO3被空气中的氧气氧化.
,工业上$\frac{n[(N{H}_{4})_{2}S{O}_{3}]}{n(C{u}^{2+})}$采用0.6最为适宜,此时(NH4)2SO3略过量,其原因是保证生成的CuCl不被氧气氧化或(NH4)2SO3被空气中的氧气氧化.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 A1/MnO4-电池是一种高能电池,以Ga2O3为缓蚀剂,其示意图如图所示.已知电池总反应为Al+MnO4-+2H2O═Al(OH)4-+MnO2.下列说法正确的是( )
A1/MnO4-电池是一种高能电池,以Ga2O3为缓蚀剂,其示意图如图所示.已知电池总反应为Al+MnO4-+2H2O═Al(OH)4-+MnO2.下列说法正确的是( )| A. | 电池工作时,K+向负极移动 | |
| B. | 电池工作时,Al电极周围溶液pH增大 | |
| C. | 正极反应为MnO4-+2H2O+3e-═MnO2+4OH- | |
| D. | 电池工作时,电子由Al经溶液流向Ni |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com