
�����������ʣ���KI ��ͭ ��ϡ���� ��NH3 ��NaHSO4 ��Ba(OH)2 �������������� �ఱˮ
��1�������ʵķ������д����Ŀհ״�(�����ʱ��)
| ����� | ����� | �� | �ǵ���� | ����� |
| ���ڸ�������� |
��2������ij������������Һ�пɷ������ӷ�Ӧ��H����OH��= H2O��д�������ӷ�Ӧ��Ӧ�Ļ�ѧ����ʽ ��
��3�����ʢٵ�ϡ��Һ�ڿ����б����������������Һ����ɫ����Ӧ�����ӷ���ʽΪ ��
 ��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����Ȼ�������ý���������ֱ�ӷ�Ӧ�Ƶõ��ǣ� ��
A��CuCl2 B��MgCl2 C��NaCl D��FeCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��22.4g��Fe2O3��Cu�Ļ�����м���0.5mol/L��������Һ600mLʱ������ǡ����ȫ�ܽ⣬������Һ�в���Fe3+�����ù�����CO�ڸ����»�ԭ��ͬ������ԭ����������ٵ�����Ϊ
A��6.4g ������ �� B��4.8g���������� C��2.4g ���� ���� D��1.6g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ���ǣ� ��
A��������ͼ�Ԫ�صĻ����ﲻһ�����к�ǿ�Ļ�ԭ��
B��Ԫ�صĵ���һ������������ԭ��Ԫ�صĻ������Ƶ�
C��������ֻ�ܵõ��ӱ���ԭ��������ֻ��ʧ���ӱ�����
D���ڻ�ѧ��Ӧ�У��õ���Խ������������������Ծ�Խǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���н�����ʵ�ķ���ʽ����ȷ���ǣ� ��
A����0.1 mol/L�İ�ˮ��pHΪ11�� NH3��H2O  NH4+ +OH��
NH4+ +OH��
B����Na�����ˮ�У��������壺2Na+2H2O= 2OH��+2Na++H2��
C��AlƬ����NaOH��Һ�У��������壺2Al+2OH��+2H2O = 2AlO2�� +3H2��
D����CuCl2��Һ��������ʵ�飬���ݷ��⣺CuCl2  Cu2+ +2 Cl��
Cu2+ +2 Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ɫ��ѧ���Ի�ѧ��Ӧ����ˡ�ԭ�Ӿ����ԡ�(ԭ�ӽ�Լ) �ĸ��Ҫ������ġ�ԭ�Ӿ����ԡ���Ӧ�У�ԭ�Ϸ����е�����ԭ��ȫ��ת��������������������ʵ�����ŷš����·�Ӧ�з��ϡ�ԭ�Ӿ����ԡ����� �� ��
A. �Ҵ�����������ȩ B.�Ҵ���Ũ���Ṳ������ϩ
C.����ϩ��һ���������ƾ۱���ϩ D.������������Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ�����ӷ���ʽ��ȷ���� ( )
A����������������������Һ��Ӧ��CH3COOCH2CH3 �� OH-���� CH3COO- + CH3CH2O- + H2O
B��������Һ������������ͭ��Ӧ��2H����Cu(OH)2 ���� Cu2+��2H2O
C����������Һ��ͨ������������̼��2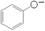 ��CO2��H2O
��CO2��H2O 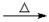 2
2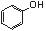 ��CO
��CO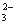
D����ȩ��Һ������������ͭ����Һ����CH3CHO+2Cu(OH)2+OH_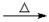 CH3COO��+ Cu2O��+ 3H2O
CH3COO��+ Cu2O��+ 3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ȫ������(C3F8)��һ���������塣�����й�ȫ�������˵���У�����ȷ����
A��ȫ������ĵ���ʽΪ
B����ͬѹǿ�µķе㣺C3F8��C3H8
C��C3F8����������̼ԭ�� ����ͬһֱ����
����ͬһֱ����
D��ȫ����������м��м��Լ����зǼ��Լ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��д��ȷ���ǣ��� ��
��A��̼�����ˮ�⣺HCO3��+H2O  H3O++CO32��
H3O++CO32��
��B������������Һ�м��������ˮ��Ag����NH3��H2O��AgOH����NH4��
��C��Ũ�Ⱦ�Ϊ0.1mol��L-1������������Һ��̼�������Һ��������
Ba2++2OH��+NH4++ HCO3��=BaCO3��+NH3��H2O+H2O
��D�������������Һ��ͨ������SO2���壺ClO����SO2��H2O��HClO��HSO3��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com