
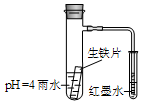
| A.生铁片中的碳是原电池的阳极,发生还原反应 |
| B.雨水酸性较强,生铁片仅发生析氢腐蚀 |
| C.墨水回升时,碳极反应式为:O2 + 2H2O + 4e—= 4OH— |
| D.具支试管中溶液pH逐渐减小 |
科目:高中化学 来源:不详 题型:单选题
| A.本质是:M + nH2O = M(OH)n + n/2 H2↑ |
| B.电化学腐蚀必须在酸性条件下进行 |
| C.化学腐蚀比电化学腐蚀更普遍 |
| D.本质是:M – ne- = Mn+[ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜锌原电池中铜是负极 | B.用电解法精炼粗铜时粗铜作阴极 |
| C.在镀件上电镀铜时可用金属铜作阳极 | D.电解稀硫酸制H2、O2时铜作阳极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
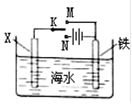
| A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀,采用了牺牲阳极的阴极保护法 |
| B.若X为锌棒,开关K置于N处,X极的反应:4OH--4e-=O2↑+2H2O |
| C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀,采用了外加电流的阴极保护法 |
| D.若X为碳棒,开关K置于M处,X极的反应:O2+4e-+2H2O=4OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe-2e=Fe2+ | B.2H2O+O2+4e=4OH- | C.4OH- -4e=2H2O+O2 | D.2H++2e=H2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe-2e- | B.2H2O+O2+4e- |
| C.2Fe+2H2O+O2 | D.Fe-3e- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.用惰性电极电解饱和氯化钠溶液的总反应为:2Cl- + 2H+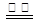 H2↑+ Cl2↑ H2↑+ Cl2↑ |
| B.锌铜原电池中盐桥中的阴离子移向ZnSO4溶液 |
| C.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
| D.电镀时,镀层金属作阳极;精炼铜时,用纯铜作阴极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解熔融的氧化铝制取金属铝,用铁作阳极 |
| B.电解法精炼粗铜,用纯铜作阴极 |
| C.钢铁吸氧腐蚀的正极反应:O2 +2H2O+4e---=4OH— |
| D.在镀件上电镀锌,用锌作阳极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe -2e-= Fe2+ | B.Fe -3e- = Fe3+ |
| C.O2 +2H2O +4e- = 4OH- | D.2H+ + 2e- = H2 ↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com