
| A. | 10mL 0.5mol/L CH3COONa溶液与6mL 1mol/L盐酸混合:c(Cl-)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | 等浓度的下列稀溶液:①硫酸氢钠 ②乙酸钠 ③醋酸 ④碳酸氢钠 ⑤硝酸钠 ⑥苯酚钠,它们的pH由小到大排列为:③⑤①④②⑥ | |
| C. | 常温下0.1 mol/L的下列溶液 ①NH4Al(SO4)2 ②NH4Cl ③NH3•H2O ④CH3COONH4中c (NH4+)由大到小的顺序是:②>①>④>③ | |
| D. | 在25℃时,将a mol•L-1的氨水与0.01 mol•L-1的盐酸等体积混合反应时溶液中c(NH4+)=c(Cl-).用含a的代数式表示NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$ |
分析 A.反应后溶质为0.005mol醋酸、0.001molHCl和0.005molNaCl,醋酸部分电离,溶液显示酸性,由于氢离子来自HCl、水和醋酸的电离,则c(H+)>c(CH3COO-);
B.先按照物质的类别分为碱、盐、酸进行分类,在此基础上主要考虑盐的水解,判断盐溶液的酸碱性再进行比较;
C.①铝离子水解抑制铵根离子的水解;②铵根离子水解;③弱碱电离,且电离的程度很弱;④醋酸根离子水解促进铵根离子水解;
D.c(NH4+)=c(Cl-),根据电荷守恒可知:c(H+)=c(OH-),NH3•H2O的电离常数Kb=$\frac{[N{{H}_{4}}^{+}][O{H}^{-}]}{[N{H}_{3}•{H}_{2}O]}$进行计算.
解答 解:A.10mL 0.5mol/L CH3COONa溶液中含有0.005mol醋酸钠,6mL 1mol/L盐酸中含有0.006molHCl,两溶液混合后溶质为0.005mol醋酸、0.001molHCl和0.005molNaCl,醋酸部分电离,溶液显示酸性,由于氢离子来自HCl、水和醋酸的电离,则c(H+)>c(CH3COO-),则溶液中正确的离子浓度大小为:c(Cl-)>c(Na+)>c(H+)>c(CH3COO-)>c(OH-),故A错误;
B.等浓度时,①硫酸氢钠相当于一元强酸,③醋酸为一元弱酸,⑥苯酚钠、④碳酸氢钠、②乙酸钠水解都呈碱性,且水解程度依次减小,所以溶液pH⑥>④>②,⑤硝酸钠溶液呈中性,pH=7,所以溶液pH由小到大的顺序为,①③⑤②④⑥,故B错误;
C.同浓度的下列溶液:①NH4Al(SO4)2②NH4Cl③NH3•H2O,④CH3COONH4,因①中铝离子水解抑制铵根离子的水解;②中铵根离子水解;③弱碱电离,且电离的程度很弱;④醋酸根离子水解促进铵根离子水解,则c(NH4+)由大到小的顺序是:①>②>④>③,故C错误;
D.由溶液的电荷守恒可得:c(H+)+c(NH4+)=c(Cl-)+c(OH-),已知c(NH4+)=c(Cl-)=0.005mol/L,则有c(H+)=c(OH-)=1×10-7mol/L,所以溶液显中性;电离常数只与温度有关,则此时NH3•H2O的电离常数Kb=$\frac{[N{{H}_{4}}^{+}][O{H}^{-}]}{[N{H}_{3}•{H}_{2}O]}$=$\frac{0.005×1×1{0}^{-7}}{\frac{a}{2}-0.005}$=$\frac{1{0}^{-9}}{a-0.01}$,故D正确;
故选D.
点评 本题考查了离子浓度大小比较,题目难度中等,涉及盐的水解原理、溶液pH的判断、离子浓度大小比较、电离平衡常数的计算等知识,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及灵活应用基础知识都能力,明确电荷守恒、物料守恒的含义是判断离子浓度大小的关键.


科目:高中化学 来源: 题型:解答题
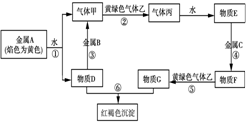 现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、红褐色沉淀H,已知黄绿色气体乙为Cl2,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出),请根据以上信息回答下列问题:
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、红褐色沉淀H,已知黄绿色气体乙为Cl2,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出),请根据以上信息回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
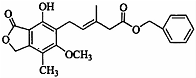
| A. | 分子中所有的原子共平面 | |
| B. | 既可以与FeCl3溶液发生显色反应.又可以与NaHCO3溶液反应放出CO2气体 | |
| C. | 1 mol该化合物最多可以与9mol H2发生加成反应 | |
| D. | 该物质能发生取代反应、氧化反应、加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙中加入盐酸:CO32-+2H+═CO2↑+H2O | |
| B. | 向NaOH溶液中通入足量CO2:CO2+OH-═HCO3- | |
| C. | FeBr2溶液中通入足量氯气:Fe2++2Br-+2 Cl2═Fe3++Br2+4Cl- | |
| D. | 硫酸铜溶液与氢氧化钡溶液混合:Cu2++2OH-═Cu(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除①③⑤ | B. | 除③⑤⑥ | C. | ②④⑦ | D. | ①②④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl溶液在电流作用下电离出自由移动的离子 | |
| B. | 设阿伏加德罗常数为NA,则2.24LCO2气体中所含原子数目为0.3NA | |
| C. | 实验室里将少量金属钠保存在煤油中 | |
| D. | 向某无色溶液中加入少量BaCl2溶液,生成不溶于稀硝酸的白色沉淀,则此溶液中一定有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KBr、KI(含 淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.(已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O)
化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KBr、KI(含 淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.(已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com