
����Ŀ�����ݵ�����Դ����������Ṥҵ���û�����(��Ҫ�ɷ�ΪFeS2)��Ϊԭ�ϡ����������գ�
(1)��0.050mol SO2(g) ��0.030mol O2(g) ����һ��2L���ܱ������У���һ�������·�����Ӧ��2SO2(g)+O2(g)2SO3(g)+Q����2���ӷ�Ӧ�ﵽƽ�⣬���n(SO3)=0.040mol����O2��ƽ����Ӧ����Ϊ______
(2)���ݻ�����ʱ�����д�ʩ�����������SO2ƽ��ת���ʵ���______(ѡ����)
a.�Ƴ����� b.�����¶�
c.��Сѹǿ d.�ٳ���0.050molSO2(g)��0.030molO2(g)
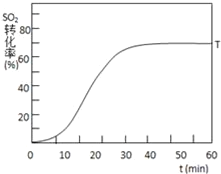
(3)����ʼ�¶�T1(673K)ʱSO2��ת�����淴Ӧʱ��(t)�ı仯��ͼ������ͼ�л�������������������£���ʼ�¶�ΪT2(723K)ʱSO2��ת�����淴Ӧʱ��仯��ʾ��ͼ___
(4)��������һ�����������յIJ���ΪSO2��Fe3O4
�ٽ�����������ղ���Fe3O4����H2SO4�������ۣ����Ʊ�FeSO4�����ܹ�������ά����Һ���㹻�����ԣ���ԭ����______
��FeS2�ܽ���Һ�е�Fe3+��ԭΪFe2+������������ΪSO42����д���йص����ӷ���ʽ______����2mol������������ʱת�Ƶĵ�����Ϊ______
���𰸡�0.005mol/(Lmin) bd 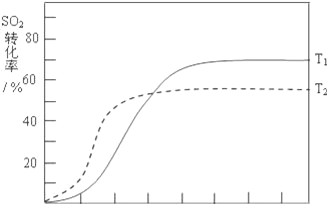 ����Fe3+��Fe2+��ˮ�⣬����ֹFe2+��������Fe3+ FeS2+14Fe3++8H2O=15Fe2++2SO42��+16H+ 14NA
����Fe3+��Fe2+��ˮ�⣬����ֹFe2+��������Fe3+ FeS2+14Fe3++8H2O=15Fe2++2SO42��+16H+ 14NA
��������
(1)����v��![]() ������������ʣ�Ȼ���������֮�ȵ��ڶ�Ӧ���ʵĻ�ѧ������֮�ȼ��㣻
������������ʣ�Ȼ���������֮�ȵ��ڶ�Ӧ���ʵĻ�ѧ������֮�ȼ��㣻
(2)��Ӧ���ȣ�Ϊ���SO2ƽ��ת���ʣ�Ӧʹƽ��������Ӧ�����ƶ����ɽ����¶ȣ�������䣬���ܴ�ѹǿ�ĽǶȿ��ǣ�������Ӱ��ƽ���ƶ����Ƴ�������ƽ�����淴Ӧ�����ƶ������������SO2ƽ��ת���ʣ��ɴ˷������
(3)��Ӧ�Ƿ��ȷ�Ӧ���¶����ߣ�ƽ��������У����������ת���ʼ�С�����ﵽƽ������Ҫ��ʱ�����̣��ݴ˻������ߣ�
(4)��Fe3����Fe2����ˮ�⣬Fe2���ױ�������Fe3����
�ڸ���������ԭ��Ӧ�еķ�Ӧ��������X�ε����غ�����ƽ��ѧ����ʽ����Ϸ��̼���ת�Ƶ�������
(1)v(SO3)��![]() ��
�� ��0.01mol/(Lmin)������v(O2)��
��0.01mol/(Lmin)������v(O2)��![]() v(SO3)��0.005mol/(Lmin)���ʴ�Ϊ��0.005mol/(Lmin)��
v(SO3)��0.005mol/(Lmin)���ʴ�Ϊ��0.005mol/(Lmin)��
(2)a���Ƴ�������ƽ�������ƶ������������ת���ʼ��٣��ʲ�ѡ��
b�������¶ȣ�ƽ�������ƶ������������ת��������ѡ��
c����Сѹǿ��ƽ�������ƶ������������ת���ʼ��٣��ʲ�ѡ��
d���ٳ���0.050molSO2(g)��0.030molO2(g)���൱������ѹǿ��ƽ�������ƶ������������ת��������ѡ��
�ʴ�Ϊ��bd��
(3)��Ӧ��2SO2(g)+O2(g)2SO3(g) ��H��0��SO2��ת��������ʼ�¶�T1��673K���淴Ӧʱ��(t)�ı仯��ͼ�������������䣬���ı���ʼ�¶�ΪT2��723K���¶����ߣ�ƽ��������У����������ת���ʼ�С������Ӧ�������ﵽƽ����Ҫ��ʱ��̣���ͼ�л����¶�T2��SO2��ת�����淴Ӧʱ��仯��Ԥ�ڽ��ʾ��ͼ��ͼ��ʾ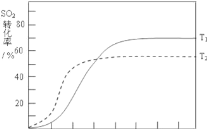 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
(4)��Fe2O3(��Fe3O4��)����H2SO4�����ɵ�Fe3����Fe2����ˮ�⣬Fe2���ױ�������Fe3��������Ҫ����Fe�ۺ��ᣬ����Fe3����Fe2����ˮ�⣬����ֹFe2����������Fe3�����ʴ�Ϊ������Fe3����Fe2����ˮ�⣬����ֹFe2����������Fe3����
��2�۵������Ӿ��л�ԭ�ԣ�FeS2���Խ���Һ�е�Fe3����ԭΪFe2����������������Ϊ��������ӣ��йص����ӷ���ʽΪ��FeS2+14Fe3++8H2O=15Fe2++2SO42��+16H+��������������������ӣ���2mol���������ʱת�Ƶĵ�����Ϊ14NA���ʴ�Ϊ��FeS2+14Fe3++8H2O=15Fe2++2SO42��+16H+��14NA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ���Ũ�ȵ�NaOH��Na2CO3�Ļ����Һ�м���ϡ���ᣮ�������ӷ���ʽ��������ʵ�������
A.OH��+2CO32��+3H+��2HCO3��+H2O
B.2OH��+CO32��+3H+��HCO3��+2H2O
C.2OH��+CO32��+4H+��CO2��+3H2O
D.OH��+CO32��+3H+��CO2��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(N2H4)�ʹ�������(NaH2PO2)������ǿ��ԭ��.�����Ź㷺����;��
(1)��֪:��N2H4(l)+O2(g)=N2(g)+2H2O(g) ��H=-621.5 kJ��mol-1
��N2O4(l)-=N2(g)+2O2(g) ��H2=+204.3 kJ��mol-1
����ȼ�ϵ�ȼ�շ�ӦΪ2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ��H=_____.
(2)��֪��ӦN2H4(g)+ 2Cl2(g)![]() N2(g)+4HCl(g),T��Cʱ,��V L�����ܱ������м���2 mol N2H4(g)��4 mol Cl2(g) ,���Cl2��HCl��Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��
N2(g)+4HCl(g),T��Cʱ,��V L�����ܱ������м���2 mol N2H4(g)��4 mol Cl2(g) ,���Cl2��HCl��Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��
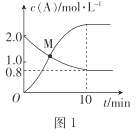
��0~ 10 min��,��N2(g)��ʾ��ƽ����Ӧ����v(N2)=_______��
��M��ʱ,N2H4��ת����Ϊ______(��ȷ��0.1)%��
��T ��Cʱ,�ﵽƽ�������������м���1.2 mol N2H4(g)��0.4 mol Cl2(g)��0. 8 mol N2 (g)��1.2 mol HCl(g) ,��ʱƽ��______(���������ƶ����������ƶ����������ƶ���)��
(3)���ڶ���������,������(P4)��ʯ�����̼������Һһͬ��������黯��Ӧ�����Ƶ�NaH2PO2,ͬʱ����������(PH3)����,�÷�Ӧ�Ļ�ѧ����ʽΪ________________��
�ڴ�����(H3PO2)��һԪ�ᣬ������.1.0 mol��L-1��NaH2PO2��ҺpHΪ8,��������Ka=___________��
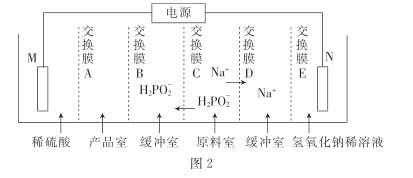
���ô�������ͨ�����������Ʊ�������.װ����ͼ2��ʾ������ĤA����____(������������������������)����Ĥ,�缫N�ĵ缫��ӦʽΪ______,����·������3.8528��105���ص���ʱ.�Ƶô���������ʵ���Ϊ_____ (һ�����ӵĵ���Ϊ 1.6��10- 19����,NA��ֵԼΪ6. 02�� 1023)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Inorganic Syntheses��(���ϳ�)һ���У���һ��ͼ��ʾ��װ�ã������Ʊ�ij�ָ���Ĵ������塣��װ������װ��ҩƷ��ȷ����(����)
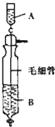
A.A��װŨ���ᣬB��װŨ����
B.A��װŨ���ᣬB��װŨ����
C.A��װ��������Ũ��Һ��B��װŨ��ˮ
D.A��װŨ��ˮ��B��װ��������Ũ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ľṹ��ͼ��ʾ�����ڿ��������������ȷ����( )
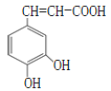
A.����ʽΪC9H8O4
B.1mol�������������4mol���������ӳɷ�Ӧ
C.����ˮ�����ܷ���ȡ����Ӧ���ܷ����ӳɷ�Ӧ
D.�ܻ�ԭ����KMnO4��Һ��˵��������к���̼̼˫��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������һ�����Ƴ���������ҩ����ɰ�����(![]() )�ͼ״���Ӧ�Ƶá����������գ�
)�ͼ״���Ӧ�Ƶá����������գ�
(1)д������������Ľṹ��ʽ��_______________________________��
(2)��ҵ����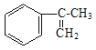 �����IJ���ͬ���͵ķ�Ӧ�Ƶð����ᡣ�밴ʵ�ʽ��еķ�Ӧ˳��д��ָ����Ӧ����������Ҫ���Լ��ͷ�Ӧ������
�����IJ���ͬ���͵ķ�Ӧ�Ƶð����ᡣ�밴ʵ�ʽ��еķ�Ӧ˳��д��ָ����Ӧ����������Ҫ���Լ��ͷ�Ӧ������
��һ��________________________________�� �ڶ���________________________________��
(3)д�����IJ���Ӧ�Ļ�ѧ����ʽ_______________________________________________��
(4)A�DZ� ������̼ԭ�ӵ�һ��ͬϵ���A������̼ԭ�ӿ��Դ���ͬһƽ���ϡ�д��A�Ľṹ��ʽ________________________________��
������̼ԭ�ӵ�һ��ͬϵ���A������̼ԭ�ӿ��Դ���ͬһƽ���ϡ�д��A�Ľṹ��ʽ________________________________��
(5) ![]() �ǰ����������ij��ͬ���칹���һ�ȴ��������������������Һ���ȣ����ɵ��л�����Ľṹ��ʽΪ_____________________________________��
�ǰ����������ij��ͬ���칹���һ�ȴ��������������������Һ���ȣ����ɵ��л�����Ľṹ��ʽΪ_____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ϡHNO3��Cu��ȡ����NO����֤�������������ʵ�װ�ã�����˵��������ǣ�������

A.���ռ�������NaOH��ҺB.�Թ��ϲ�������ʼ��Ϊ��ɫ
C.С�Թ�����Һ���ճ���ɫD.��ֽ�ȱ�����ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ĺ�ҵ�Ʊ��������ĺϳɡ����Ĵ������������Ũ���ȹ��̣�������м��㣺
��1�����ü���Ķ���ת���������Ʊ�������
��һ��ת���Ļ�ѧ����ʽ��CH4+H2O��CO+3H2��
�ڶ���ת���Ļ�ѧ����ʽ��2CO+CH4+2O2��3CO2+2H2��2CO+O2��2CO2��
���б�״����1m3�ļ��飬����һ��ת��80%���ڶ���ת��20%������������ȫת������Եõ�H2__mol��
��2���ñ���K2CO3��Һ����������������е�CO2�Եõ�����������������������CO2������Ҫ����K2CO3��Һ____g������֪��20��K2CO3�ܽ�ȣ�110g/100gˮ��
��3����֪NH3+2O2��HNO3+H2O�����а���1.7�֣�������ˮ�������Ͽ��Ƶ������Ũ��Ϊ___%���ڸ������м���__��ˮ���տɵ�50%�����ᣮ
��4����ҵ�ϳ���98%��ŨH2SO4��Ϊ��ȡŨHNO3����ˮ����63.5%HNO3������ΪM1���м�98%��ŨH2SO4������ΪM2�������ֱ�õ�97.7%��HNO3��49%��H2SO4��Һ������HNO3����
�������������HNO3��H2SO4��H2O������ģ�������ǰ��Ͷ�ϱ�![]() ��ֵ__����ʽ���㣩��
��ֵ__����ʽ���㣩��
����������У���H2O�����ռ��������5.0%�����У�M1+M2����5.0%��H2O��ʧ����Ͷ��ʱ��![]() ��ֵ��α仯������ʽ����˵��__��
��ֵ��α仯������ʽ����˵��__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾΪij�¶�ʱBaSO4�ij����ܽ�ƽ������,����˵������ȷ����( )
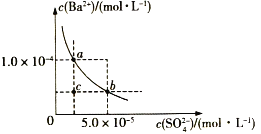
A.����Na2SO4(s)��ʹ��Һ��a���Ϊb��
B.�������Ϸ�����(��������)����һ��ʱ,����BaSO4��������
C.�����ܼ�����ʹ��Һ��c���Ϊ������a��b֮���ijһ��(����a��b)
D.�����¶�,��ʹ��Һ��b���Ϊc��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com