
 元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A. | 非金属性:Z<T<X | B. | R与Q的电子数相差26 | ||
| C. | 气态氢化物稳定性:R<T<Q | D. | 最高价氧化物的水化物的酸性:T>Q |
分析 R单质在暗处与H2剧烈化合并发生爆炸,R为F元素,由元素在周期表中的位置可知,T为Cl元素,Q为Br元素,X为S元素,Z为Ar元素,结合元素周期律解答.
解答 解:R单质在暗处与H2剧烈化合并发生爆炸,R为F元素,由元素在周期表中的位置可知,T为Cl元素,Q为Br元素,X为S元素,Z为Ar元素,
A.Z为Ar元素,最外层为稳定结构,金属性与非金属性在同周期中最弱,同周期自左而右金属性减弱,故非金属性Z<X<T,故A错误;
B.R为F元素,Q为Br元素,原子序数相差26,故B正确;
C.同主族自上而下,非金属性减弱,故非金属性F>Cl>Br,非金属性越强,气态氢化物越稳定,故稳定性HF>HCl>HBr,故C错误;
D.同主族自上而下,非金属性减弱,故非金属性Cl>Br,非金属性越强,最高价氧化物的水化物的酸性越强,故酸性:T>Q,故D正确;
故选BD.
点评 本题考查元素周期表与元素周期律等,难度不大,推断R为氟元素是关键,注意掌握元素周期律.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:解答题
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | +4、-2 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
 ,其中所含的化学键类型为离子键和非极性键.
,其中所含的化学键类型为离子键和非极性键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤⑥ | B. | ②⑦ | C. | ①③④ | D. | ⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核内质子数为131 | B. | 核内中子数为131 | C. | 原子序数为53 | D. | 质量数为53 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
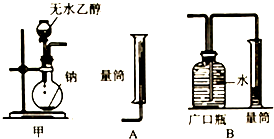
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广使用燃煤脱硫技术,防止SO2污染 | |
| B. | 采用绿色化学生产工艺,提高原子利用率 | |
| C. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| D. | 加大石油、煤炭的开采力度,增加化石燃料的供应量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,4.48LCH3CH2OH中约含有1.204×1023个羟基 | |
| B. | 常温常压下,31g白磷P4和红磷P8的混合中约含有6.02×1023个磷原子 | |
| C. | 标准状况下,7.8g苯中约含有1.806×1023个碳碳双键 | |
| D. | 1molH2O2在MnO2催化作用下完全反应转移的电子数约为1.204×1024个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向硫酸铜溶液中加入过量的NaHS溶液:Cu2++2HS-→CuS↓+H2S↑ | |
| B. | Fe3O4溶解在过量的稀硝酸中:Fe3O4+8H+→Fe2++2Fe3++4H2O | |
| C. | 碳酸氢铵溶液与苛性钾溶液混和共热:NH4++OH-→NH3↑+H2O | |
| D. | 将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O→SO32-+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com