
| A. | 甲烷→一氯甲烷 | B. | 氯乙烯→聚氯乙烯 | ||
| C. | 乙醇→乙醛 | D. | 对苯二甲酸,乙二醇→聚酯纤维 |
分析 A、甲烷与氯气反应生成一氯甲烷,同时生成HCl;
B、氯乙烯发生加聚反应生成聚氯乙烯;
C、乙醇制取乙醛,同时生成水;
D、对苯二甲酸与乙二醇发生缩聚反应生成聚酯纤维,同时生成水.
解答 解:A、甲烷与氯气反应生成一氯甲烷,同时生成HCl,原子没有全部利用,故A错误;
B、氯乙烯发生加聚反应生成聚氯乙烯,原子利用率是100%,故B正确;
C、乙醇制取乙醛,同时生成水,原子没有全部利用,故C错误;
D、对苯二甲酸与乙二醇发生缩聚反应生成聚酯纤维,同时生成水,原子没有全部利用,故D错误;
故选B.
点评 绿色化学实质是原子利用率是100%,全部转变成所需要的产物,从源头上做起,不浪费、不污染.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | Cu与浓HNO3→Cu(NO3)2 | B. | Cu与稀HNO3→Cu(NO3)2 | ||
| C. | Cu$→_{△}^{O_{2}}$CuO$\stackrel{稀HNO_{3}}{→}$Cu(NO3)2 | D. | Cu+AgNO3→Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
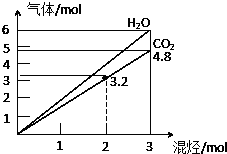 两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是| A. | ②⑤ | B. | ②④ | C. | ③④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 完全燃烧产物只有二氧化碳和水 | |
| B. | 它们几乎不溶于水 | |
| C. | 分子的通式为CnH2n+2,与氯气发生取代反应 | |
| D. | 它们完全由碳氢元素组成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 4种 | C. | 2种 | D. | 1种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
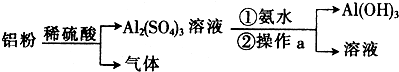
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含氧酸的酸性H3ZO4>H2YO4>HXO4 | |
| B. | 非金属性X<Y<Z | |
| C. | 元素的负化合价的绝对值按X、Y、Z减小 | |
| D. | 气态氢化物的稳定性按X、Y、Z的顺序减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大于14NA | B. | 等于14NA | C. | 小于14NA | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═2HClO+CaSO3↓ | |
| B. | 足量铁屑溶于稀硫酸:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-═CO32-+H2O | |
| D. | 铝片溶于烧碱溶液:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com