
某同学在实验报告中有以下实验数据:①用托盘天平称取11.7 g食盐;②用量筒量取5.26 mL盐酸;③用广泛pH试纸测得溶液的pH值是3.5,其中数据合理的是( )
A.① B.②③ C.①③ D.②
科目:高中化学 来源: 题型:
2013年全国各地都遭遇“十面霾伏”。其中,机动车尾气和燃煤产生的烟气对空气质量恶化贡献较大。
⑴汽车尾气净化的主要原理为:2NO(g) + 2CO(g) 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0
若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。
(下图中υ正、K、n、w分别表示正反应速率、平衡常数、物质的量、质量分数)

(2)机动车尾气和煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOX可以消除氮氧化物的污染。已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
2NO2(g) N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol
H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
 写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式: 。
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式: 。
(3)用NH3催化还原NOX也可以消除氮氧化物的污染。右图,采用NH3作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物转化率),
反应原理为:
NO(g) +NO2(g)+2NH3(g) 2N2(g) + 3H2O(g)。
2N2(g) + 3H2O(g)。
①该反应的△S 0,△H 0(填“>”、“=”或 “<”)。
②对于气体反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作KP),
则上述反应的KP= 。
③以下说法正确的是 。
 A.第②种催化剂比第①种催化剂脱氮率高
A.第②种催化剂比第①种催化剂脱氮率高
B.相同条件下,改变压强对脱氮率没有影响
C.催化剂①、②分别适合于250℃和450℃左右脱氮
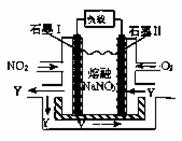
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理见右图。该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应为 。
(5)硝酸工业尾气中氮氧化物(NO和NO2)可用尿素〔CO(NH2)2〕溶液除去。反应生成对大气无污染的气体。1 mol尿素能吸收工业尾气中氮氧化物(假设NO、NO2体积比为1:1)的质量为___________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验误差分析错误的是
A.用润湿的pH试纸测稀碱溶液的pH,测定值偏小
B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D.测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度差值偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
普伐他汀是一种调节血脂的药物,其结构如右图所示(未表示出其空间构型)。下列关于普伐他汀的性质描述正确的是
A.不能通过反应形成高分子化合物
B.不能使酸性KMnO4溶液褪色
C.能发生加成、取代、消去反应
D.1mol该物质最多可与1molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各为1.5mol,Mg2+为0.5mol,则SO42-的物质的量为………………………………………………………………( )
A.0.1mol B.0.5mol C.0.15mol D.0.25mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是………………………………………………….………( )
A.H2SO4的摩尔质量是98
B.等质量的O2和O3中所含的氧原子数相同
C.等质量的CO与CO2中所含碳原子数之比为11︰7
D.将98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列物质中所混有的少量杂质,写出有关的反应方程式。
(1)铜粉中混有少量铝粉 ;
(2) FeCl3中混有少量FeCl2 ;
(3)Na2CO3中混有少量NaHCO3 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列方法中,不能用于实验室制取氨气的是
A.将烧瓶中的浓氨水加热
B.将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中
C.在烧瓶中将熟石灰和氯化铵混合,加水调成泥状后加热
D.加热试管中的氯化铵固体
查看答案和解析>>
科目:高中化学 来源: 题型:
800℃时,在2L密闭容器内,发生反应:2NO(g)+O2(g) 2NO2(g),已知在此体系中, n(NO)随时间的变化如表:
2NO2(g),已知在此体系中, n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)已知升高温度,NO2的浓度减小,则该反应是 (填“吸”或“放”)热反应。
(2)该反应平衡常数K的表达式为 。
(3)右图中表示NO2的变化的曲线是 。

用O2表示从0~2 s内该反应的平均速率v= 。
(4)为使该反应的反应速率增大,且平衡向正反应方向
移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com