
【题目】一定温度下,某体积不变的密闭容器进行的可逆反应:3A(s) ![]() 2B(g)+C(g),下列各关系中能说明反应已达到平衡状态的是
2B(g)+C(g),下列各关系中能说明反应已达到平衡状态的是
A. 生成 B和C的速率比为2:1 B. 生成2n摩尔B同时生成n摩尔C
C. 混合气体的平均分子量不变D. 混合气体的密度不变
【答案】D
【解析】
达到平衡状态时正、逆反应速率相等,正、逆反应速率相等是指用同一种物质来表示的反应速率,不同物质表示的反应速率与化学计量数成正比。
A项、生成B的速率和生成C的速率均为正反应速率,生成B和C的速率比为2:1不能表示正、逆反应速率相等,不能说明反应已达到平衡状态,故A错误;
B项、生成2n摩尔B和生成n摩尔C均表示正反应速率,不能表示正、逆反应速率相等,不能说明反应已达到平衡状态,故B错误;
C项、反应物A为固体,生成物B和C均为气体,且物质的量比恒定为2:1,混合气体的平均分子量为定值,则混合气体的平均分子量不变不能说明反应已达到平衡状态,故C错误;
D项、反应物A为固体,生成物B和C均为气体,平衡形成过程中气体质量增大,体积不变的密闭容器中混合气体的密度增大,则混合气体的密度不变能说明反应已达到平衡状态,故D正确。
故选D。


科目:高中化学 来源: 题型:
【题目】某种光电池的工作原理为:AgCl(s)+Cu+(aq)![]() Ag(s)+Cu2+(aq)+Cl-(aq)。图为该光电池发电装置电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图,下列叙述正确的是
Ag(s)+Cu2+(aq)+Cl-(aq)。图为该光电池发电装置电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图,下列叙述正确的是

A. 光电池工作时,Ag极为电流流出极,发生氧化反应
B. 制氢装置溶液中K+移向A极
C. 光电池中工作时,Pt电极发生的反应为:2Cl--2e-=Cl2↑
D. 制氢装置工作时,A极的电极反应式为:CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化钠在无机制备、废水处理等领域常用作沉淀剂,其水溶液称为“臭碱”。可在特殊条件下以硫酸钠固体与炭粉为原料制备:Na2SO4+2C![]() Na2S+2CO2↑
Na2S+2CO2↑

(1)硫化钠固体在保存时需注意________,原因是________。
(2)实验室用上图装置以Na2SO4与炭粉为原料制备Na2S并检验气体产物、进行尾气处理。步骤如下:
①连接仪器顺序为________(按气流方向,用小写字母表示);
②检查装置气密性;③________;
④加热,进行实验。
(3)若 a mol Na2SO4和2 a mol C按上述步骤充分反应,实际得到Na2S小于amol,则实验改进方案是________。
某同学从氧化还原角度分析固体产物中可能含有少量Na2SO3,请设计实验证明其猜测是否合理(供选择的试剂有:酚酞溶液、硝酸、稀盐酸、蒸馏水) ________。
(4)经实验测定,硫酸钠与炭粉在一定条件下反应还可生成等物质的量的两种盐和体积比为1︰3的CO2和CO两种气体。反应方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+、Mg2+、SO42-而进行下列五项操作,其中正确的操作顺序是( )
①过滤
②加过量NaOH溶液
③加适量盐酸
④加过量Na2CO3溶液
⑤加过量BaCl2溶液
A.①④②⑤③B.④①②⑤③C.⑤②①④③D.②⑤④①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示。下列说法正确的是

A. H2O2分解属于吸热反应
B. 加入催化剂,减小了反应的热效应
C. 加入催化剂,可提高正反应的活化能
D. 反应物的总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将V1mL 1.0 mol·L-1硫酸溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是 ( )

A. 做该实验时环境温度为22℃B. 该实验表明热能可以转化为化学能
C. NaOH溶液的浓度约是3.0 mol·L-1D. 该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究化学反应的快慢和限度具有十分重要的意义。回答下列问题:
(1)反应2SO2(g) + O2(g)![]() 2SO3(g)是制备硫酸的重要反应,该反应为放热反应。降低温度,逆反应的速率_________;使用催化剂V2O5,正反应的速率__________ (以上填“增加”、“不变”或“减小”)。
2SO3(g)是制备硫酸的重要反应,该反应为放热反应。降低温度,逆反应的速率_________;使用催化剂V2O5,正反应的速率__________ (以上填“增加”、“不变”或“减小”)。
(2)常温下,实验室用100 mL 6.0 mol·L-1硫酸跟足量锌粉反应制取氢气。
①为降低反应进行的速率,又不影响生成氢气的量,可向反应物中加入____(填序号 )。
A.CH3COONa固体 B.KNO3固体
C.K2SO4溶液 D.KHSO4溶液
②向溶液中滴加少量硫酸铜溶液,反应速率加快,原因是___________________。
(3)一定温度下,在体积固定的密闭容器中,有色气体N与无色气体M的物质的量随时间变化曲线如图所示。反应达平衡的时间是____________,该反应的化学方程式可表示为______________________________,
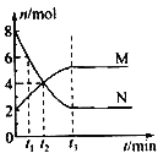
下列说法中能够判定该反应处于平衡状态的是______________(填 序号)
A.容器的压强不再变化 B.气体的颜色不再变化
C.每反应2 mol的N生成1 mol的M D.气体的密度不再发生变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com