

| A. | 和金属钠反应键①断裂 | |
| B. | 在铜催化下和O2反应键①③断裂 | |
| C. | 乙醇与金属钠反应比水与金属钠反应缓慢 | |
| D. | 钠与乙醇反应时,钠熔化成一个小球在乙醇表面不断的游动 |
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液保存在配有玻璃塞的细口瓶中 | |
| B. | 金属钠通常密封保存在煤油中 | |
| C. | 氯水通常保存在棕色细口瓶并置于阴凉处 | |
| D. | 氢氟酸保存在塑料试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖由碳、氢、氧三种元素组成 | |
| B. | 葡萄糖分子中含有 6 个碳原子和 6 个水分子 | |
| C. | 葡萄糖属于有机化合物 | |
| D. | 葡萄糖的相对分子质量为 180 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )的同分异构体有多种.符合下列条件的同分异构体有( )种
)的同分异构体有多种.符合下列条件的同分异构体有( )种| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
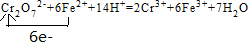 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com