NA为阿伏加德罗常数,且已知C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l)△H=-1300kJ?mol-1,则下列说法正确的是( )
A.当有20NA个电子转移时,放出2600kJ 热量
B.当有2NA个碳氧双键形成时,放出1300kJ热量
C.若生成NA个水蒸气分子焓变为△H1,则△H1<△H
D.上述反应为吸热反应
【答案】
分析:A、当有20N
A个电子转移时,转移电子物质的量为20mol,反应中氧元素化合价由0价降低为-2价,故参加反应的氧气的物质的量为
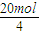
=5mol,结合热化学方程式中的反应热计算;
B、1个CO
2分子中含有2个C=O双键,有2N
A个C=O双键形成,说明有0.5molCO
2生成,结合热化学方程式中的反应热计算;
C、气态水的能量比液态水的能量该,故生成气态水放出的热量少,反应热△H
1增大;
D、该反应的反应热符号为“-”,为放热反应.
解答:解:A、当有20N
A个电子转移时,转移电子物质的量为20mol,反应中氧元素化合价由0价降低为-2价,故参加反应的氧气的物质的量为
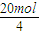
=5mol,由热化学方程式可知2.5mol氧气反应放出热量为1300kJ,故当有20N
A个电子转移时,放出的热量为1300kJ×
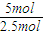
=2600kJ,故A正确;
B、1个CO
2分子中含有2个C=O双键,有2N
A个C=O双键形成,说明有0.5molCO
2生成,由热化学方程式可知2molCO
2生成放出热量为1300kJ,2N
A个C=O双键形成时,放出热量为1300kJ×
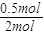
=325kJ,故B错误;
C、气态水的能量比液态水的能量该,故生成气态水放出的热量少,反应热△H
1增大,故C错误;
D、该反应的反应热符号为“-”,为放热反应,故D错误;
故选A.
点评:本题考查反应热的有关计算,难度中等,正确从微观结构判断参加反应物质的物质的量是做本题的关键,注意C选项中比较考虑符号.

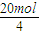 =5mol,结合热化学方程式中的反应热计算;
=5mol,结合热化学方程式中的反应热计算;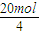 =5mol,由热化学方程式可知2.5mol氧气反应放出热量为1300kJ,故当有20NA个电子转移时,放出的热量为1300kJ×
=5mol,由热化学方程式可知2.5mol氧气反应放出热量为1300kJ,故当有20NA个电子转移时,放出的热量为1300kJ×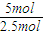 =2600kJ,故A正确;
=2600kJ,故A正确;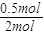 =325kJ,故B错误;
=325kJ,故B错误;

 教学练新同步练习系列答案
教学练新同步练习系列答案