
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16 g白色沉淀,在所得的浊液中逐滴加入1 mol·L1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示。
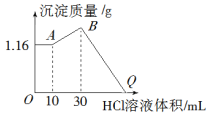
请回答下列问题:
(1)写出混合物溶于水时发生反应的离子方程式 。
(2)B点的沉淀物的化学式为 。
(3)原混合物中AlCl3的物质的量为 ,NaOH的质量为 。
(4)Q点加入的HCl溶液体积为 。
【答案】(7分)(1)Mg2++2OH![]() Mg(OH)2↓,Al3++4OH
Mg(OH)2↓,Al3++4OH![]()
![]() +2H2O(2分)
+2H2O(2分)
(2)Mg(OH)2、Al(OH)3(1分)
(3)0.02 mol(1分) 5.20 g(1分)
(4)130 mL(2分)
【解析】(1)向所得滤液中加入盐酸时,0~A段没有沉淀生成,说明溶液中NaOH过量,则铝离子完全转化为偏铝酸根离子,溶液中存在的沉淀为Mg(OH)2,反应的离子方程式为:Mg2++2OH![]() Mg(OH)2↓,Al3++4OH
Mg(OH)2↓,Al3++4OH![]()
![]() +2H2O。
+2H2O。
(2)A~B段,盐酸和偏铝酸钠反应生成氢氧化铝沉淀。
(3)A点沉淀的是氢氧化镁,则n[Mg(OH)2]= ![]() =0.02 mol,根据Mg原子守恒得n(MgCl2)=n[Mg(OH)2]=0.02 mol;A~B段,盐酸和偏铝酸钠反应生成氢氧化铝沉淀,离子方程式为H2O+
=0.02 mol,根据Mg原子守恒得n(MgCl2)=n[Mg(OH)2]=0.02 mol;A~B段,盐酸和偏铝酸钠反应生成氢氧化铝沉淀,离子方程式为H2O+![]() +H+
+H+![]() Al(OH)3↓,根据HCl溶液的体积知,n(
Al(OH)3↓,根据HCl溶液的体积知,n(![]() )=n(HCl)=1 mol/L×(0.03-0.01)L=
)=n(HCl)=1 mol/L×(0.03-0.01)L=
0.02 mol,根据铝原子守恒得n(AlCl3)=n(![]() )=0.02 mol。原混合物中n(NaOH)=n(NaCl) =n(Cl)= 2n(MgCl2)+ 3n(AlCl3)+ n(HCl)=0.02 mol×2+0.02 mol×3+0.03 L×1 mol·L1 =0.13 mol,质量为0.13 mol×40 g/mol=5.20 g。
)=0.02 mol。原混合物中n(NaOH)=n(NaCl) =n(Cl)= 2n(MgCl2)+ 3n(AlCl3)+ n(HCl)=0.02 mol×2+0.02 mol×3+0.03 L×1 mol·L1 =0.13 mol,质量为0.13 mol×40 g/mol=5.20 g。
(4)B~Q段过程中,氢氧化镁和氢氧化铝都与盐酸反应生成氯化铝和氯化镁,所以Q点溶液中的溶质是氯化铝、氯化镁和氯化钠,实际上相当于氢氧化钠和盐酸的反应,所以二者恰好反应时:n(NaOH)=n(HCl),则V(HCl)=![]() =0.13 L=130 mL。
=0.13 L=130 mL。


科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)为白色粉末,微溶于水。常用作有机合成催化剂,并用于颜料、防腐等工业。实验室可采用亚硫酸钠还原氯化铜的方法制备氯化亚铜,主要流程如图所示:

(1)上述方法制备氯化亚铜的化学方程式为_________________。
(2)下图是加热蒸发滤液,回收Na2SO4的装置。装置图中存在一处严重错误,该错误是_____________。

(3)洗涤产品氯化亚铜沉淀的试剂是___________,检验沉淀是否洗涤干净的方法是_______________。
(4)CuCl的盐酸溶液能吸收一氧化碳而生成氯化羰基亚铜[Cu2Cl2(CO)2·2H2O]。下图是用CO(含有CO2杂质)还原CuO并验证其氧化产物的实验装置图。

装置A中盛装的是饱和NaOH溶液,该装置的作用是_____________,装置B盛有澄清的石灰水,其中装置B的作用是___________,盛装CuCl的盐酸溶液的装置是____________(选填装置中提供的装置字母代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将后者逐渐滴入(或通入)前者至过量,有沉淀产生且最终消失的是( )
A. 氯化铝、氨水 B. 氢硫酸、氧气
C. 硫酸铝、氢氧化钠 D. 氯化亚铁、氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质间的归类正确的是( )
A.1H、2H、3H互为同素异形体
B.碳酸氢钠和纯碱是同一物质
C.乙醇(CH3CH2OH)与甲醚(CH3OCH3)互为同分异构体
D.O2与O3互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中都是既含有离子键又含有共价键的一组是( )
A.NaOH、H2O、NH4Cl
B.KOH、Na2O2、(NH4)2S
C.MgO、CaBr2、NaCl
D.Na2SO4、HCl、MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,质量相同的CO2、H2、O2、CH4、SO2五种气体,下列说法错误的是
A.所占的体积由大到小的顺序是:H2>CH4>O2>CO2>SO2
B.所含分子数由多到少的顺序是:H2>CH4>O2>CO2>SO2
C.密度由大到小的顺序是:SO2>CO2>O2>CH4>H2
D.所含的电子数由多到少的顺序是:CO2>SO2>CH4>O2>H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①液态HCl ②NaHCO3 ③NaCl溶液 ④CO2 ⑤蔗糖晶体 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧NH3·H2O ⑨空气 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-===H2O,该反应的化学方程式为_____________________。
(2)⑩在水中的电离方程式为___________________________。
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能
治疗胃酸过多,请写出其反应的离子方程式:________________________;如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式:________________________。
(4)写出下列反应的离子方程式
向Ba(OH)2溶液中逐滴加入稀硫酸________________________。
向Ba(OH)2溶液中通入过量的CO2_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com