
科目:高中化学 来源:辽宁省沈阳四校协作体2011-2012学年高二上学期期中考试化学试题 题型:022
| |||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源:2011-2012学年辽宁省沈阳四校协作体高二上学期期中考试化学试卷 题型:填空题
(16分)已知二元酸H2A在水中存在以下电离:H2A===H++HA-, HA-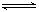 H++A2-,试回答下列问题:
H++A2-,试回答下列问题:
(1)NaHA溶液呈________性,理由是 。
(2)某温度下,向10 mL 0.1 mol/L NaHA溶液中加入0.1 mol/L KOH溶液V mL至中性,此时溶液中以下关系一定正确的是________(填写字母)。
| A.c(Na+)+c(K+)=c(HA-)+c(A2-) | B.水的离子积KW=c 2(OH-) 2(OH-) |
| C.V=10 | D.c(K+)<c(Na+) |
 已知难溶物CaA在水中存在溶解平衡;CaA(s)
已知难溶物CaA在水中存在溶解平衡;CaA(s) 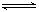 Ca2++A2-;ΔH>0。
Ca2++A2-;ΔH>0。查看答案和解析>>
科目:高中化学 来源:辽宁省期中题 题型:填空题
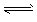 H++A2-,试回答下列问题:
H++A2-,试回答下列问题: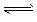 Ca2++A2-;ΔH>0。
Ca2++A2-;ΔH>0。查看答案和解析>>
科目:高中化学 来源: 题型:
已知二元酸H2A在水中存在以下电离:H2A===H++HA-, HA-![]() H++A2-,试回答下列问题:
H++A2-,试回答下列问题:
(1)NaHA溶液呈________性,理由是 。
(2)某温度下,向10 mL 0.1 mol/L NaHA溶液中加入0.1 mol/L KOH溶液V mL至中性,此时溶液中以下关系一定正确的是________(填写字母)。
A.c(Na+)+c(K+)=c(HA-)+c(A2-) B.水的离子积KW=c2(OH-)
C.V=10 D.c(K+)<c(Na+)
(3)已知难溶物CaA在水中存在溶解平衡;CaA(s) ![]() Ca2++A2-;ΔH>0。
Ca2++A2-;ΔH>0。
①温度升高时,Ksp________(填“增大”、“减小”或“不变”,下同)。
②向浊液中通入HCl气体,c(Ca2+)________,原因是 。
(4)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3。甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为________,Fe3+完全沉淀时溶液的pH为_______,通过计算确定上述方案______(填“可行”或“不可行”)。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
Fe在地壳中的含量虽次于铝,但铁及其化合物在生活、生产中的应用最广泛。请回答下列问题:
(1)Na2FeO4是一种高效多功能水处理剂,应用前景广阔。一种制备铁酸钠的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中正确的是
A.Na2O2在反应中只作氧化剂
B.Na2FeO4既是氧化物又是还原产物
C.O2是还原产物
D.2molFeSO4发生反应时,反应中共有8mol电子转移
(2)硫酸亚铁晶体(FeSO4·7H2O),俗称“绿矾”,常作医药上的补血剂。课外研究性小组测定某片状补血药品中铁元素的含量。实验步骤如下:

请回答下列问题:
①该小组发现将片状补血剂长时间置于空气中,表面“发黄”,请用化学方程式表示原因 。
②课外研究性小组发现在滤液A中滴入少量KClO溶液,并加入适量硫酸,溶液立即变黄。
甲同学推测该反应的还原产物有两种可能:①Cl2、②Cl-
乙同学结合甲的推测,认为其中一种可能可以排除,你认为可以排除的是(填序号) ;用离子方程式说明理由 。
③若该实验温度下,上述红褐色难溶物质的溶度积为![]() 试计算该物质沉淀完全所需要的pH= (要求保留2位有效数字)(已知溶液中离子浓度小于10-5mol/L时,该离子可看做沉淀完全,lg2=0.3)
试计算该物质沉淀完全所需要的pH= (要求保留2位有效数字)(已知溶液中离子浓度小于10-5mol/L时,该离子可看做沉淀完全,lg2=0.3)
④若实验过程中无损耗,最后称量得到mg红棕色的固体,则每片补血剂中含铁元素的质量为 g(用含m的式子表示)
⑤丙同学认为蒸干灼烧溶液B,也可以制得红棕色固体C,请结合化学方程式加以说明
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com