
【题目】下列过程中,涉及化学变化的是
A. 自来水通过蒸馏变成可饮用的瓶装蒸馏水
B. 夜幕降临,珠江两岸霓虹灯通电后发出美丽的亮光
C. 漂白的草帽久置空气中变黄
D. 湿衣晾干
科目:高中化学 来源: 题型:
【题目】下列做法体现环境保护理念的有( )
A.将废旧电池扔入垃圾桶
B.将实验室废液集中进行无害化处理
C.将造纸厂的污水直接排放
D.夏季将空调温度设置在26℃以上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)温室效应是导致海平面上升的主要原因,引起温室效应的人为因素主要是 。
(2)为了控制温室效应,各国科学家提出了不少方法和设想。有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底,以减小大气中CO2的浓度。为使CO2液化,可采用的措施是 (填字母)。
A.减压、升温 B.增压、升温
C.减压、降温 D.增压、降温
(3)科学家致力于二氧化碳的“组合转化”技术研究,把过多的二氧化碳转化为有益于人类的物质。如将CO2和H2以1∶4的比例混合,通入反应器。在适当的条件下反应,可获得一种重要的能源。请完成以下化学方程式CO2+4H2![]() +2H2O。 若将CO2与H2混合,在一定条件下以1∶3的比例发生反应,可生成某种重要的化工原料和水,该化工原料可能是 (填字母)。
+2H2O。 若将CO2与H2混合,在一定条件下以1∶3的比例发生反应,可生成某种重要的化工原料和水,该化工原料可能是 (填字母)。
A.甲烷 B.乙烯 C.乙醇 D.苯
(4)下列措施能快速、有效地减缓大气中CO2增加的是 。
A.使用天然气等燃料
B.控制全球人口增长
C.植树造林,保护森林
D.立即减少煤和石油的燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2中含有少量HCl气体,要想除去HCl气体,最好选用( )
A. 饱和Na2CO3溶液 B. 饱和石灰水
C. 饱和NaHCO3溶液 D. 浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温度下,体积均为1L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)![]() 2NH3(g) △H= -92.6 kJ / mol。测得数据如下表:
2NH3(g) △H= -92.6 kJ / mol。测得数据如下表:
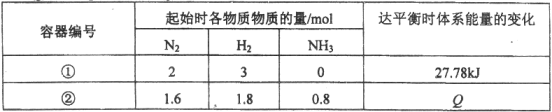
下列叙述不正确的是
A.容器②中反应开始时v(正)> v(逆)
B.容器①、②中反应达平衡时压强相等
C.容器②中反应达平衡时,吸收的热量Q为9.26 kJ
D.若条件为“绝热恒容”,容器①中反应达平衡时n (NH3)< 0.6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢俗名双氧水,医疗上利用它有杀菌消毒的作用来清洗伤口。有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。
(1)配平下列化学反应,并用单线桥表示电子转移的方向和数目:(配平和单线桥各占分数)
[ ]H2O2+[ ]Cr2(SO4)3+[ ]KOH→[ ]K2CrO4+[ ]K2SO4+[ ]H2O
(2)如消除采矿业胶液中的氰化物(如KCN,C为+2价),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,
试指出A的化学式 ,如此反应中有6.72L(标准状况)气体生成,转移电子数目为 (用NA表示)。
(3)高锰酸钾也可用于医学杀菌消毒。根据反应条件可判断氧化剂的氧化能力的强弱:例如:
MnO2+4HCl(浓)![]() MnCl2+C12↑+2H2O;
MnCl2+C12↑+2H2O;
2KMnO4+16HCl(浓)=2MnCl2+5C12↑+8H2O。
则Mn02、KMnO4氧化性 强。
某强酸反应体系中,反应物和生成物共六种物质或离子:O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2 只发生了如下过程:H2O2→O2.则该反应中发生还原反应的过程是:_________→_________,该反应应选择的酸是:_________(填序号)。
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸
(4)用0.2 mol/L Na2SO3溶液32 mL,还原含4×10-3 mol XO42-的溶液,过量的Na2SO3用0.2mol/L KMnO4酸性溶液氧化(其中KMnO4被还原成Mn2+),共消耗KMnO4溶液0.8 mL,则元素X在还原产物中的化合价是( )
A.+1 B.+2 C.+3 D.+4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com