

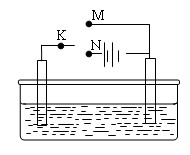
 处。
处。科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| 序号 | 反应 | 化学平衡常数 |
| 1 | Au + 6HNO3(浓) Au(NO3)3 + 3NO2↑+ 3H2O Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl- =" " AuCl4- | >>1 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 ,电解质溶液为KOH溶液;其电极反应分别是:
,电解质溶液为KOH溶液;其电极反应分别是: ══
══
 ══
══ 。下列叙述正确的是( )
。下列叙述正确的是( )| A.锌为正极 | B.放电时,负极区溶液的pH增大 |
| C.锌为负极 | D.放电时,正极区溶液的pH减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.覆盖油漆 | B.覆 盖塑料 盖塑料 | C.电镀金属 |
D.电化学保护法 E.制成不锈钢 E.制成不锈钢 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.粗铜精炼时,把粗铜接在电源的负极 |
| B.充电时,把铅蓄电池的负极接在外电源的正极 |
| C.镀锡铁破损后铁更易被腐蚀 |
D.碱性氢氧燃料电池工作时,负极反应为:   |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com