

分析 海水晒盐得到卤水,通入氯气氧化溴离子得到低浓度的溴单质溶液,通入热空气吹出溴单质,用纯碱溶液吸收辐射反应得到溴酸根离子、溴离子的溶液,再用硫酸酸化得到溴单质;在卤水中加入熟石灰沉淀镁离子生成氢氧化镁沉淀,过滤后再氢氧化镁沉淀中加入盐酸溶解得到氯化镁溶液,浓缩蒸发结晶析出氯化镁晶体,在氯化氢气流中失去结晶水得到固体氯化镁固体,电极熔融氯化镁得到金属镁,
(1)步骤II中是碳酸钠吸收溴单质生成溴酸钠、溴化钠和二氧化碳,步骤III中是溴酸钠和溴化钠在卤水溶液中发生归中反应生成溴单质;
(2)从卤水到MgCl2(aq)经历了氯化镁沉淀为氢氧化镁,过滤后得到氢氧化镁沉淀溶解在盐酸中得到氯化镁溶液,目的是浓缩溶液富集镁离子;
(3)根据能和金属镁发生反应的气体来回答.
解答 解:(1)步骤II中是碳酸钠吸收溴单质生成溴酸钠、溴化钠和二氧化碳,反应的离子方程式为:3Br2+3CO32-═BrO3-+5Br-+3CO2,步骤III中是溴酸钠和溴化钠在卤水溶液中发生归中反应生成溴单质,反应的离子方程式为:BrO3-+5Br-+6H+═3Br2+3H2O,
故答案为:3Br2+3CO32-═BrO3-+5Br-+3CO2;BrO3-+5Br-+6H+═3Br2+3H2O;
(2)制备镁的工艺中,从卤水到MgCl2(aq)经历MgCl2→Mg(OH)2→MgCl2的过程,生成Mg(OH)2的过程是镁的富集,
故答案为:镁的富集;
(3)能和金属镁发生反应的气体:氮气、氧气、二氧化碳,Ar气体是惰性气体不和镁反应,所以可以用氩气做镁蒸气的冷却剂,
故选A;
故答案为:A.
点评 本题主要考查了海水资源的综合利用,海水提溴工艺,氯碱工业,实验基本操作,题目难度中等.


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA | |
| B. | 14g分子式为CnH2n的链烃中含有的C-H键的数目为2NA | |
| C. | 室温时,1.0 L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| D. | Fe与水蒸气反应生成22.4L氢气,转移电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某中学化学兴趣小组同学为探究元素周期律,设计了如下一系列实验.
某中学化学兴趣小组同学为探究元素周期律,设计了如下一系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和苯都能和溴水发生化学反应而使溴水褪色 | |
| B. | 乙烷可使酸性高锰酸钾溶液褪色 | |
| C. | 糖类和蛋白质都是高分子化合物 | |
| D. | 乙酸和油脂都能与氢氧化钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
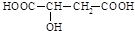
| A. | ①②③ | B. | ①②③④ | C. | ①②③⑤ | D. | ①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com